|
��2017��12�µ�һ����Ʒ���һ�������۳ƺ�������CFDA��CDE��̷�����ʮ�����α��Ƽ��������ظ�Ŀ¼��ע����������ģ�ļ�������2��14������������ʮ�����α��Ƽ���ڶ���ͨ��һ��������Ʒ��Ŀ¼�������ļ�����Ӱ�컯ѧҩ����ҩע���һ�������۵��걨������������������Ҫ������
2018��2�·�����ͨ������ҩ��������Чһ��������Ʒ��Ŀ¼���ڶ�����
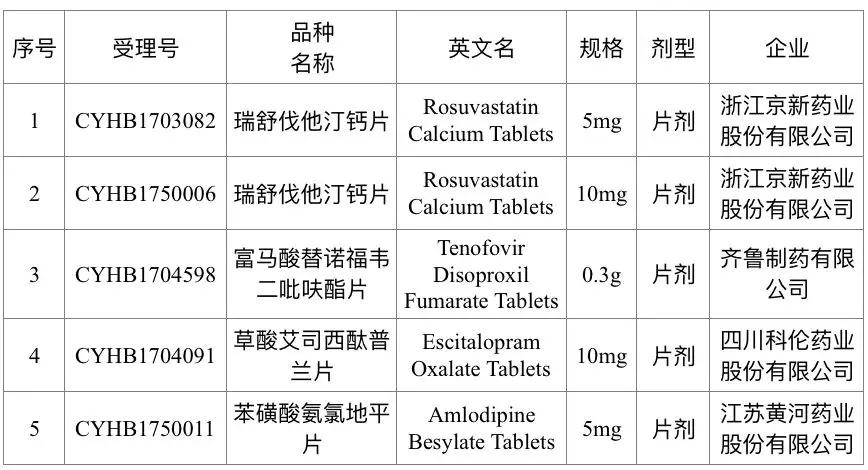
ע���������ᰱ�ȵ�ƽƬΪ289Ŀ¼Ʒ��
��������1 ԭ�еز���Ҫ��Ҫ��BE��
�����ӷ���ҩ�α��Ƽ�Ŀ¼����ʮһ������CFDA��ʼ����������α��Ƽ���ԭ�еز�����Ʒ��������2018��2��14��Ϊֹ��46��ԭ�еز�����Ʒ��ʽ��Ϊ�α��Ƽ��������Ŵ���������Ƭ�����������ຽ��ҡ���������Ƭ�������ᰱ�ȵ�ƽƬ����ɳ̹���ҡ�������ͪƬ����ʯ���������Ƭ������ù��Ƭ������ͪ��Ī��ƽƬ�������������Ƭ��������ɳ��Ƭ����������Ƭ�����˿��Ƭ����������Ƭ����������Ƭ������ʯɢ18����Ʒ����289Ŀ¼�IJ�Ʒ��ԭ�еز�����Ʒ����α��Ƽ����������ҩ�������ң�����������ȥ����ɹ�ԭ��ҩ��
��1��46��ԭ�еز����α��Ƽ�
|
Ŀ¼����
|
ҩƷͨ������
|
��֤��
|
|
��ʮһ��
|
��������Ƭ
|
�ݶ�ҽҩ��������˾
|
|
����ɳ̹��Ƭ
|
��һ������ҩ���Ϻ�������˾
|
|
�����ᰱ�ȵ�ƽƬ
|
������ҩ����˾
|
|
������ͪƬ
|
������ɭ��ҩ����˾
|
|
�����в���Ƭ
|
�������ҩƷ����˾
|
|
���ܰ�Ƭ
|
���ģ��й���ҩҵ����˾
|
|
��ʯ���������Ƭ
|
��˹������ҩ����˾
|
|
����ɳ̹��Ƭ
|
�������ҩƷ����˾
|
|
����ù��Ƭ
|
�Ϻ�������ҩ����˾
|
|
����ͪƬ��
|
������ɭ��ҩ����˾
|
|
��������Ƭ
|
�Ϻ����ָ����ҩҵ����˾
|
|
����ʯɢ
|
����-�������������ҩ����˾
|
|
��Ī��ƽƬ
|
�ݶ�ҽҩ��������˾
|
|
���������嶡��Ƭ
|
ʩά�ţ������ҩ����˾
|
|
ͷ�߿��彺��
|
����������ҩ����˾
|
|
���ᱴ������Ƭ
|
����ŵ����ҩ����˾
|
|
�����������Ƭ
|
���ģ��й���ҩҵ����˾
|
|
���������ຽ���
|
������ɭ��ҩ����˾
|
|
�����������Ƭ
|
ʩά�ţ������ҩ����˾
|
|
�����������Ƭ
|
�Ϻ�������ҩ����˾
|
|
���������ƿ���
|
��������ҩ����˾
|
|
�Ŵ���������Ƭ
|
ʩά�ţ������ҩ����˾
|
|
������ɳ��Ƭ
|
��һ������ҩ������������˾
|
|
��ʮ����
|
��������Ƭ
|
�㽭��ڣ��ҩ����˾
|
|
���з���͡��Ƭ
|
������ҩ����˾
|
|
��˾��������þ����Ƭ
|
��˹������ҩ����˾
|
|
���˿��Ƭ
|
�Ϻ�������ҩ����˾
|
|
��������ŵ��Τ������Ƭ��
|
������ʷ�ˣ��������˾
|
|
��������Ƭ
|
��ŵ�ƣ���������ҩ����˾
|
|
�������ػ���Ƭ
|
ʩά�ţ������ҩ����˾
|
|
�����������Ƿ�Ƭ
|
������ҩ����˾
|
|
��������Ƭ
|
�Ϻ�������ҩ����˾
|
|
���������Ƭ
|
��һ������ҩ���Ϻ�������˾
|
|
��������Ƭ
|
�ݶ�ҽҩ���Ϻ�������˾
|
|
���������Ŵ�����Ƭ
|
ʩά�ţ������ҩ����˾
|
|
ͷ�߿���ɻ�����
|
����������ҩ����˾
|
|
����������ົ���Ƭ
|
ʩά�ţ������ҩ����˾
|
|
��ʮ����
|
��������ɽ��������Ƭ
|
��˹������ҩ����˾
|
|
������͡�ƻ���Ƭ
|
����ŵ����ҩ����˾
|
|
���������ܽ���
|
�������ҩƷ����˾
|
|
�����ز�����Ƭ
|
��˹������ҩ����˾
|
|
�����������
|
��һ������ҩ������������˾
|
|
��ȷ�Ƭ
|
����ŵ����ҩ����˾
|
|
������Ƭ
|
������ɭ��ҩ����˾
|
|
��ɳ̹����
|
����ŵ����ҩ����˾
|
|
����������
|
������ɭ��ҩ����˾
|
��������Դ���̴�����V3.5��
��ע��“��”���з���ҩ���һ�������۳ƺţ�
����ԭ��ҩѡ��ز��������������Ϊ��Ӧ��һ�������������������ķ���ҩ����ѹ��������ҩ����ԭ��ҩͬ��һ��������ξ����۸���ԭ��ҩ�����DZ�Ȼ���ƣ�ԭ�еز���������ԭ��ҩ���������ɱ������籽���ᰱ�ȵ�ƽƬ������ͪƬ��������ŵ��Τ������Ƭ�����з���ҩ��һ�������ۡ���������������Ʒ������ʯɢ�����з���͡��Ƭ����������Ƭ����������Ƭ�����������Ƭ����������ƬҲ���з���ҩ�걨һ�������ۡ�
������ǰ������һ��Ҫ��ԭ�еز���ҲҪ��������Ч�����飬����Ҳ��2017��12�¹����˻�����������ĺ��������������ᰱ�ȵ�ƽƬBE�о������ò�Ʒ�ڷ���ҩ�α��Ƽ�Ŀ¼����ʮһ�����й�ʾΪԭ�еز��α��Ƽ�������ȷ�Ϸ���ҩһ��������BE�����ѱ������⡣����������δ����������������ֹ�����顣�ɴ˿����������������������ش�����ԭ�еز�����������BE��
����2���ظ�Ŀ¼��289��Ʒ�Ƿ�չһ�������ۣ�
����һ��������289Ŀ¼�IJ�Ʒ����CFDA���������ظ�ҩƷ�IJ�Ʒ��93����ѧ�ɷ�164����Ʒ��ռ��57%����ô����164����Ʒ�Ƿ���Ҫ��չһ���������أ�
����һ����ԣ������ظ�Ŀ¼��Ʒ�����Ϊ�����ż��ϵ͵IJ�Ʒ�����ǣ���8����Ʒ�Ƚ����⣬����289Ŀ¼���������������ظ�ҩƷ��������289��ҩĿ¼�еĹ�������Ʒ��������Ʒ���ֱ��ǣ������ʲ�Ƭ��������Ѫƽ�������Ƭ��������ѪƽƬ��������������Ƭ��������ɽݹ�м�Ƭ������ɽݹ�м�Ƭ������С��Ƭ������С��Ƭ����8����Ʒ��Ҫ�����ҩ��������Чһ�������۰칫��һ����֯ר����ѯ�ᣬ������۷����м�������ȷ�������⡣Ԥ�ƴ����ƷԸ�չһ�������۵���ҵҲ���࣬���ܳɹ����һ�������۵ģ�Ԥ����ӵ�нϴ��г�DZ���IJ�Ʒ��
�������2��ʾ����89����ѧ�ɷ�160��289Ŀ¼��Ʒ�����������ظ�Ŀ¼�У��������۹�ģ�ϴ�İ��ȵ�ƽ��������ƽ������˫�ҡ��������塢������ɳ�ǡ�����ù�ء�ͷ����������������ù�ء����������ȡ����а��ȵ�ƽ������˫�ҡ��������塢ͷ��������������Ͱ���ù�أ���Ŀǰһ���������ٴ�������ҵ�������϶�IJ�Ʒ�����а��ȵ�ƽ��ͷ����������ҵ���һ�������۳ƺš�
��2�������ظ�Ŀ¼�е�289Ŀ¼��Ʒ
|
Ŀ¼
|
��ѧ�ɷ�
|
|
�����ظ�Ŀ¼������
|
��Ī���֡���Ī���ֿ���ά��ء�����ù�ء���˾ƥ�֡�����Ʒ��������Τ���������ȵ�ƽ��������������˾�������������������ơ�����˾͡�������������������������ҡ����ض������������ɡ������������ӡ�������ͪ���������ء�����˫�ҡ���Ī�涡����̪����������ס�������ມ����������ʲݡ������ǰ��ׇf������Ѫƽ����������������������ມ��������塢��������ء���ù�ء����Һ�ù�ء�����ɳ�ǡ������������հ�����������顢������ƽ����������������ù�ء�����ù�ء������涡������Τ�֡�����ƽ���ȱ��������ȱ�ມ��Ȼ��ء������������������������ʯ����Ī��ƽ����Ⱥ��ƽ��ŵ��ɳ�ǡ�����ά�֡������ɡ���������ơ�������ͪ������������⻯�ɵ��ɡ�������ມ�ɽݹ�м˫�ȷ����ơ�˫�״�Ī��̼�����ơ�������ມ�������ͷ�߰��С�ͷ�����ơ�ͷ��������ά����B2��ά����B6��������ƽ��������ɽ�桢С�������͡����ȥ�����ᡢ�强�¡�Ҷ�ᡢ�����������Ұ����������ມ������¡��Ŵ�������������ɳ��
|
|
����ڶ��������ظ�Ŀ¼
|
����Ӣ�ơ��ȵ�ƽ�������
|
|
������������ظ�Ŀ¼
|
�������
|
��������Դ���̴�����V3.5��
��������ҵĿǰ����һ�������۵������������г�DZ���ϴ��Ҽ�����Խϳ���IJ�Ʒ�������Ƿ��ڹ����ظ�Ŀ¼�ڣ����ǹ��ڷ����ȵ㡣�����Ʒδ���п�����Ϊһ�������ۻ�õ���ҵ���϶࣬���г��۸�ƫ�ͣ��Ӷ�������ҵ�ܻ�õ��г���ģ���ޡ�
��������3 �г���ģС�IJ�Ʒ�Ƿ����ֻ����ҵ����
����2018��2�£�CDE�������ڹ�������ѧҩƷ����ҩע����������ģ��һ����Ҫ�������֪ͨ��Ŀǰ���������ǿڷ��Ƽ���ע��������Ҫ�����ٹ�ģ��
�������ݡ���ѧҩƷ����ҩע����������ģ��һ����Ҫ���ڷ��Ƽ�����ͨƬ��/���Ҽ���������Ƭ�����Ҽ��ȣ�ע����������Ӧ���ٴﵽ�ⶨ��ҵ��������ģ��10%��100,000�Ƽ���λ��������ѡ����ġ��ڷ��Ƽ���ɢ��/��Һ��/������/������/�ǽ�����Ҫ��ע����������Ӧ���ٴﵽ�ⶨ��ҵ��������ģ��10%���ڷ��Ƽ��Ļ�����Ƭ��/����ע����������Ӧ�����ٴﵽ10����Ƽ���λ�����ҽ���ע����������ģ���ⶨ��ҵ��������ģһ�¡�
����10����Ƽ���λ�����й�ҩ��2015����IJ���ҩ���Ƽ������������öȺ������Ч������ָ��ԭ��9011�����ᵽ��“����ҩƷӦ����һ��������������ģ1/10�����Σ���10�����λ��������ѡ����ģ���������˵�����ɡ�2017��8��25��CFDA��CDE�����ġ���������һ��������BE�о���ҩƷ�����������������֪ͨ��������������ڶ���Ҳ�ᵽ��“BE�о�����ҩƷӦ������10����Ƽ���λ��������ҵ������ҵ��������ҩƷ����BE�о���”
����������Ҫ�������г�DZ���������١����������10����Ƽ���λ�IJ�Ʒ����ҵ���IJ����ܷ���Ϊע�����Ŀ����أ�
����CFDA����2015��5��6�շ����Ļ�ѧҩƷ��ע������걨����Ҫ�����У���80���ģ���Ҳ�ᵽ��“�ٴ�����/BE������Ʒ�Ĵ��������ա�������Ӧ����ҵ������һ��”��
����������ҩ��������Чһ�������������ֳ����ָ��ԭ��Ҫ��“�ֳ������������Ʒ����������Ӧ�����Ӧ�г�����ҵ��������ģ��������һ�£����������������Ч���о����ٴ��о����������۵IJ�Ʒ������ģ��������һ��”��
�����ο�FDA��1997��ָ�ϡ�Guide for Industry——TheFDA published Good Guidance Practices in February 1997���������г���ģ��С��ҩƷ�����ڷ���ҩ��صķ���Ҫ�����������10���Ƽ���λ����BE������������Ӧ���ⶨ����ҵ����һ�£�������ҵ��ϣ����С��10���Ƽ���λ����ҵ���������õ���10��������Ʒ��BE���飬����Ҫ��FDA����ҩ�칫�ҹ�ͨȷ�ϡ�
�������CFDAӲ�Թ涨Ҫ����10���Ƽ���λ����ôһЩ�������ķ�����������ޣ����㷨���϶���BE�о�����ҵ���������о�ҩƷ��ͨ��һ�������ۺ���������ۣ����������Ʒ�����Ч����Ҳ�������ꡣ
����Ϣ��Դ��ҽҩ���ñ���Top
�ְܾ칫������ʵʩ��ҽ����е�������ۼල�����취���й������֪ͨ��ʳҩ���е�ࡲ2018��31�ţ���2��27�չ�������Ҫ�������£�
��ҽ����е�������ۼල�����취��������ʳƷҩƷ�ල�����ܾ����38�ţ������¼�ơ��취�����ѷ�������2018��3��1����ʩ�С�Ϊ�᳹��ʵ���취�����й�Ҫ���ֽ��й�����֪ͨ���£�
����һ���������á��취�������᳹����ѵ����
��������ʳƷҩƷ�ල��������Ҫ�߶����ӣ����������᳹��ʵ���취����ר���ƶ������᳹��ѵ�ƻ�����ʵ���������᳹��ѵ�������ܾ�����2018��1�¶�ʡ��ʳƷҩƷ�ල�������ŵȿ�չ����ѵ��ʡ��ʳƷҩƷ�ල��������Ҫ��ǿ���С��ؼ�ʳƷҩƷ�ල�������ż���ҵ����ѵ����ع�����ָ����
����������ʵ����ҽ����е�������ۼල��������
������һ������ʳƷҩƷ�ල��������Ҫ��ʵ����ҽ����е�������ۼල�������������취��ʩ�к�Ҫ��ǿ�����������ڴ���ҽ����е�������۵���ҵ��ҽ����е���罻���������ƽ̨�ṩ�ߵļල������������ҵ��ҽ����е���罻���������ƽ̨�ṩ����ʵ�����������Ρ�
����������ʡ��ʳƷҩƷ�ල��������Ҫ���ա��취���ȹ涨Ҫ����ʵ����ҽ����е�������ۺͽ������Ϣ�Ĵ��ù�����ָ��ר�˸������ҽ����е���罻���ƽ̨��Ϣ���ա����鴦������ϴ�����ع���������2018��2��28��ǰ��ҽ����е���罻���ƽ̨ע������������ܾ���е���˾��
������������ҽ����е�������ۺ�ҽ����е���罻���������ƽ̨��������
������һ���ܾ���“ҽ����е������Ӫ���ɱ�����Ϣϵͳ”�����¼��“��Ϣϵͳ”����������ҽ����е�������ۺ�ҽ����е���罻���������ƽ̨�����ȹ��ܣ�����2018��3��1������ʽ���á�����ҽ����е�������ۺ�ҽ����е���罻���������ƽ̨�����������ҵ��ʱ����ؼ����Ա����ҵ�й���Ա�ɴӹ���ʳƷҩƷ�ල�����ܾ���վ��ҳ��http://www.sfda.gov.cn/WS01/CL0001/��“���ϰ���”��Ŀ�е�“ҽ����е������Ӫ���ɱ�����Ϣϵͳ”������롣
��������������ҽ����е�������۵���ҵ��ͨ��“��Ϣϵͳ”�����ڵ��������м�ʳƷҩƷ�ල�������Ű����������ҽ����е����������Ϣ�����������м�ʳƷҩƷ�ල�������Ŷ������Ϣ���к�ʵ�����Ϲ涨�ģ�Ӧ����7��������������ṫ��������Ϣ��
����������ҽ����е���罻���������ƽ̨�ṩ�߿�ͨ��“��Ϣϵͳ”�����ڵ�ʡ��ʳƷҩƷ�ල�������Ű����������ҽ����е���罻���������ƽ̨���������ύ��ز��ϣ�ʡ��ʳƷҩƷ�ල��������Ӧ����������ҵ�ύ���ϵ������Խ��к˶ԣ����Ϲ涨�����Ա���������ҽ����е���罻���������ƽ̨����ƾ֤���ڱ�����7��������������ṫ����ر�����Ϣ��
����Ϣ��Դ������ʳƷҩƷ�ල�����ܾ֣�Top
�ֹܾ��ڷ���������ҩ��ҩ���ٴ����鼼��ָ��ԭ���ͨ�棨2018���39�ţ���2��27�չ�����
��������ҩ��ҩ���ٴ����鼼��ָ��ԭ��ԭ�������
http://www.sda.gov.cn/WS01/CL0050/225542.html
����Ϣ��Դ������ʳƷҩƷ�ල�����ܾ֣�Top
�Ƽ��� ����������ӡ�������ҿƼ���Դ��������ƽ̨�����취����֪ͨ�����Ʒ�����2018��48�ţ���2��24�չ�����
����ƽ̨����Ҫ���������
1.Χ�ƹ���ս�����������չ��Ҫ�Ƽ���Դ���ռ������������湤����
2.�нӿƼ��ƻ���Ŀʵʩ���γɵĿƼ���Դ�Ļ㽻�������ͱ�������
3.��չ�Ƽ���Դ����Ṳ�����������Ƽ����»�ṩ��������չ��ѧ�ռ������ݴ�������������Դ��չ���Ʒ���
4.�����ά�����߷���ϵͳ����չ�Ƽ���Դ�����빲������Ӧ�ü����о���
5.��չ��Դ���ʽ����������μ���ع���ѧ����֯��ά�����������밲ȫ��
����Ϣ��Դ���Ƽ�����Top
������ҽҩ���������߷�����ල˾����ӡ������ҽҩ�ල����ָ�ϣ����棩���Ե㹤��������֪ͨ��2��24�չ���������ҽҩ�ල����ָ�ϣ����棩���Ե㹤�������в����������£�
Ŀ������
1�����顶��ҽҩ�ල����ָ�ϣ����棩�������¼�ơ�ָ�ϡ����Ŀ�ѧ�ԡ��淶�ԡ�ָ���ԣ���ȡ�õľ������������һ�������ơ�ָ�ϡ���Ϊ�����ȫ����Χ���С�ָ�ϡ��춨���û�����
2���ӿ��ƽ���ҽҩ�ලִ��������չ����ȷ��ҽҩ�ලִ��ְ�����������ȫ�����ƶȣ������ලִ��������
3��������ҽҩ�ලִ���������ۣ���ǿ��ҽҩ�ලִ���Ĺ淶�����裬����ʾ���������á�
�Ե������
������������ա����ϡ��Ĵ��������6ʡ�С�
�Ե�����
��һ����ʡ���У���ȷ�Ե�ල��������ϵ�ˡ�
��������֯��չ��ָ�ϡ��Ե㷽����ѧϰ����ѵ������
��������չ�Ե㹤������ʱ�ռ���ָ�����ù��������������⡣
���ģ�������֯�ٿ��Ե㹤���о����ƽ����飬�����ж������С�
���壩�Ե㹤��������ʱ�ϱ��Ե㹤���ܽἰ��ز��ϡ�
����Ϣ��Դ��������ҽҩ�����֣�Top
��ҵ����Ϣ�������ڹ����ڰ�����������ҵ����ҵʾ������������֪ͨ�����Ų��桲2018��36�ţ���2��24�չ�����ͬ���Ϻ���ɽ��ҵ����15����ҵ������Ϊ“��������ҵ����ҵʾ�����أ������ࣩ”����������������Է��ҵ����36����ҵ������Ϊ“��������ҵ����ҵʾ�����أ���ɫ�ࣩ”��
��֪ͨ���У�ͬ���Ϻ���ɽ��ҵ����15����ҵ������Ϊ“��������ҵ����ҵʾ�����أ������ࣩ”����������������Է��ҵ����36����ҵ������Ϊ“��������ҵ����ҵʾ�����أ���ɫ�ࣩ”��
���ڰ�����������ҵ����ҵʾ��������������ҽҩ��������ǣ�
|
���
|
�ϱ���λ
|
����ʾ����������
|
���
|
|
15
|
����ʡ����ί
|
ҽҩ·�������Ƹ۾��ü���������
|
����
|
|
30
|
ɽ��ʡ����ί
|
ҽ����е·ɽ��������������ҵ������
|
����
|
|
48
|
����ʡ����ί
|
����ҽҩ·���ݸ��¼�����ҵ������
|
��ɫ
|
����Ϣ��Դ�����Ų���Top
���ֹܾ��ڶ�ҽ�ƻ���Ӧ�ô�ͳ����������ҩ�Ƽ�ʵʩ���������Ĺ��棨2018���19�ţ���2��12�շ�������Ҫ�������£�
һ�����������涨�Ĵ�ͳ��ҩ�Ƽ�������
��һ������ҩ��Ƭ����������ˮ������ȡ�ƳɵĹ��壨�����ɢ���������������ȣ�������壨���̡���ҩ�ȣ���Һ�壨�����ȣ���ͳ���ͣ�
����������ҩ��Ƭ��ˮ��ȡ�ƳɵĿ������Լ�����ҩ��Ƭ��������ƳɵĽ��Ҽ���
����������ҩ��Ƭ�ô�ͳ������ȡ�ƳɵľƼ���������
����ҽ�ƻ����������Ĵ�ͳ��ҩ�Ƽ�Ӧ���䡶ҽ�ƻ���ִҵ����֤�������������Ʒ�Χһ�¡�������������֮һ�ģ����ñ�����
������һ����ҽ�ƻ����Ƽ�ע������취�����У����й涨�IJ�����Ϊҽ�ƻ����Ƽ��걨�����Σ�
�������������г������й�ӦƷ����ͬ�����IJ�ͬ����Ʒ�֣�
������������ҩ�䷽������
�������ģ����������Ϲ����йع涨���Ƽ���
�ġ�ҽ�ƻ������ƴ�ͳ��ҩ�Ƽ�Ӧ��ȡ�á�ҽ�ƻ����Ƽ�����֤����δȡ�á�ҽ�ƻ����Ƽ�����֤�����ߡ�ҽ�ƻ����Ƽ�����֤������Ӧ�Ƽ����͵�ҽ�ƻ�����ί�з��������ĵ�λ���ƣ�����ͬʱ��ί�з����ڵ�ʡ��ʳƷҩƷ�ල�������ű�����
����Ϣ��Դ������ʳƷҩƷ�ල�����ܾ֣�Top
���ֹܾ���������YY 0285.5—2018��Ѫ���ڵ��� һ����ʹ�������� ��5���֣��������ܵ��ܡ���16��ҽ����е��ҵ���Ĺ��棨2018���27�ţ���2��28�շ�������Ҫ�������£�
YY 0285.5—2018��Ѫ���ڵ���һ����ʹ�������� ��5���֣��������ܵ��ܡ���16��ҽ����е��ҵ���Ѿ���ͨ���������Թ���������2019��3��1����ʵʩ��
����Ϣ��Դ������ʳƷҩƷ�ල�����ܾ֣�Top
CFDA����ҩ����Ʒ�ֹ��棨�ӳ������ڵ�11�ţ���2018���25�ţ�����2��24�չ�����
���ݡ���ҩƷ�ֱ�����������ʮ�������йع涨����������ҩƷ�ֱ�������ίԱ����֯��ίԱ����������ʳƷҩƷ�ල�����ֺܾ���������5����ҵ������5����ҩ����Ʒ�ּ������豣����

����Ϣ��Դ������ʳƷҩƷ�ල�����ܾ֣�Top
CFDA����ҩ����Ʒ�ֹ��棨�ӳ������ڵ�11�ţ���2018���25�ţ�����2��24�չ�����
���ݡ���ҩƷ�ֱ����������Ĺ涨������ʳƷҩƷ�ල�����ܾ�������5����ҵ������5����ҩƷ����Ϊ����ҩ����Ʒ�֣�
|
���
|
ҩƷ����
|
��������
|
��������
|
����Ʒ�ֺ�
|
������ҵ
|
|
1
|
����ƽ������
|
2
|
2018��2��24��—2025��2��24��
|
ZYB2072017011
|
ɽ��������ҩ���Źɷ�����˾
|
|
2
|
�������
|
2
|
2018��2��24��—2025��2��24��
|
ZYB2072017012
|
����ҵ�����ţ��ɷ�����˾��������ҩ��
|
|
3
|
��ĥ���ڷ�Һ
|
2
|
2018��2��24��—2025��2��24��
|
ZYB2072017013
|
���Ϻ�ɭ��ҩ�ɷ�����˾
|
|
4
|
��յ���ص���
|
2
|
2018��2��24��—2025��2��24��
|
ZYB2072018002
|
�ϲ�����ҩҵ����˾
|
|
5
|
�Dz�Ƭ
|
2
|
2018��2��24��—2025��2��24��
|
ZYB2072018005
|
�人����ҽҩ�Ƽ���������˾
|
����Ϣ��Դ������ʳƷҩƷ�ල�����ܾ֣�Top
Ŀǰ������ҽҩ��ͨ��ҵ���жȽϵͣ��г��������ң�������ͨ��ҵ�������ӿ���ҵ���ϣ������ҵ���жȳ�Ϊҽҩ��ͨ��ҵ��չ�����ҽ�����ߵ�һ����������
��������ǿҩ����ռ9���г�
���ݹ���ʳƷҩƷ�ල�����ܾ�ͳ�ƣ�����2016��11�µף�ȫ������ҩƷ������ҵ12975�ң�ҩƷ����������ҵ5609�ң���Ͻ�ŵ�220703�ң����۵���ҩ��226331�ң�����ҩ���ŵ�����447034�ҡ�
������ȥ���꣬����ҩƷ������ҵ���жȳ�����ߡ�ǰ100λҩƷ������ҵ��Ӫҵ������ռͬ��ȫ���г��ܹ�ģ�ı��س�����������ȥ5���������1.38���ٷֵ㡣
��������������������ͳ�Ʊ��棬2016��ҩƷ������ҵ��Ӫҵ������ǰ100λռͬ��ȫ��ҽҩ�г��ܹ�ģ��70.9%�����У��ļ�ȫ����ͷ��ҵ��Ӫҵ������ռͬ��ȫ��ҽҩ�г��ܹ�ģ��37.4%��2016��ҩƷ������ҵ��Ӫҵ������ǰ100λͬ������14.0%�����У��ļ�ȫ����ͷ��ҵ��Ӫҵ������ͬ������12.2%��
������������2016��12�·����ġ�ȫ��ҩƷ��ͨ��ҵ��չ�滮��2016��2020�꣩�������¼��“���滮��”����������ȷ�������2020�꣬ҩƷ������ǿ��ҵ�����۶�ռҩƷ�����г��ܶ�90%���ϣ�����Ŀǰ����ҽ�����ߵ�����ʵ��ҩƷ������ҵ���Ͻ�һ���ӿ졣
ҽҩ������ҵ����ҵ��������Ի���Ϊȫ���Ժ�������ҽҩ������ҵ��������ҵ����ҽҩ����ҵ��Ŀǰ��ȫ�����ļ�ȫ����ҽҩ������ҵ��ͷ�����������ִ���һ�һ��߶����������ͷ��ҵ��
�������Ĵ���ͷҩ��ʵ������
�����й�ҽҩ�����ܹ�˾���������ӹ�˾��ҩ�عɹɷ�����˾ӵ��ȫ������ҩƷ�������磬��Ҫ���۰���ҩƷ��ҽ����е��ҩ����Ƭ�ȣ����۹�ģ����������ȫ��ҽҩ��ͨ��ҵ������λ�ӵ�һ��
��������ҽҩ�ع�����˾���������ӹ�˾����ҽҩ��ҵ��������˾��Ϊҽҩ��ͨ�ľ�Ӫ���壬��ȫ��30���ص�ʡ�н������������磬��2016���ҽҩ������ҵ��Ӫҵ�����������ڶ���
�����Ϻ�ҽҩ���Źɷ�����˾����2016���ҽҩ������ҵ��Ӫҵ��������������������ȫ��20���ص�ʡ�У���Ҫ�����ڻ����������ͻ�������
��������ͨҽҩ���Źɷ�����˾����Ϊ�й�������Ӫҽҩ��ͨ��ҵ����Ӫ�������Ѿ����ǹ���70%���ϵ����������볬��10������οͻ��������ȶ���ҵ���ϵ��
����4�ҹ�˾��Ϊ���Ź�˾��ҵ������ҽҩ����ҵ��Ϊ����2016��ҽҩ��ͨ���ë���ʻ���ά����6.33��7.57%������Ӫҵ��������������ë������Ӱ��ά���ڽϸ�ˮƽ��7.63��15.31%����
��������ͨ��Ŀǰ�й�������Ӫҽҩ��ͨ��ҵ��ӵ�н�Ϊ���صĿ���ģʽ——��Ҫ��Ӧ�����ն˵Ȼ���ҽ���г���ҵ��רע��ҽҩ��ͨ������������ͷ��������ģ��С�����ھ���ͨҽҩ��ҵ�������ռ��С��ë������Խϵͣ�ʹ��������Ӫҵ�����ʵ�������3�ң�Ϊ7.63%����
������Ϊҽҩ��ͨ��ҵ�ĺ��ľ�����֮һ��Ӫ������Ľ��������������������Ӱ��Ŀǰ��ҵ�ľ�����֣�����ҵ�������ϽΣ��Ӵ��Ҹ�Ч��Ӫ����������������Ǿ���ҽҩ��ͨ��ҵδ����ҵ��λ�ľ�������֮һ��
�����й�ҽҩ���ŵ�Ӫ�����簴��ȫ����ʡ���������вɹ���ϵ���衣����2016��ף��й�ҽҩ�����ڱ������Ϻ������ݼ�����������4����Ŧ��ʡ����������38�������м���������185����������������24����������251����
������������ӵ���Ƚ��IJִ������������ִ�������Ϣ����ϵͳ�Ը��������ҩƷ����ͳһ���䡣
�������⣬�й�ҽҩ���Ż���Ϊ��Ӧ�̼��ͻ��ṩ������Ӧ�̽�����������ϲ�Ʒ�������������������������Ĺ�������Ӧ���������ʷ���ȹ�Ӧ����ֵ������2017��3�µף��й�ҽҩ����ֱ���ͻ��Ѹ���ȫ��15589��ҽԺ�����ӵ�����������̿ͻ�8911�Ҽ�����ҩ��90122�ҡ�
��������ҽҩ�ع�����ҽҩ��ͨ��Ӫ���廪��ҽҩ��ҵ�����DZ���������ҽҩ��ͨ��ҵ��ӵ��7.7��ƽ����Ӫ����������������9��ƽ����ҽҩ�����������ġ�
��������ҽҩ��ҵ���ųе��˰�������14�����صĻ�ҩ���ͣ����е���ɽ�������������֡������������ϡ����յ�����150���ؼ��к��ؼ��е���������ũ�����͡�
�����Ϻ�ҽҩ���γ��Ի�����������������������Ϊ���ĵ�ȫ���Է������磬����20��ʡ�м�������������ҽ�ƻ�������2.5��ң�ҽҩ���۷ֲ���16��ʡ������������1800��ҡ�
����2016���Ϻ�ҽҩ��ɹ̶��ʲ�Ͷ��10.98��Ԫ����Ҫ����GMP���켰ҽҩ�������裬�����Ʊ������Ϻ���ȫ���������ؽ����ͬʱ�������ƽ����������кͻ��������������ĵĽ��裬��ȫ���ҹ��Ҽ�ҽҩ��������ҵ������ҵ��
��������ͨ�Ⱥ��ں��������������ϡ��Ϻ����㶫�����������յȵ�Ͷ������30��ʡ��ҽҩ�������ĺ�54�ҵ��м��������ģ�����2016��ף�����ͨ�Ѿ�������84��ҽҩ�����������ģ�ӵ������ҩ��911�ң������˵꣩��
��������ҵ�������——4+N
����������ҽҩ��ͨ����ҽҩ����Ϊ������˾����������ҩҵ�ɷ�����˾��ҩ����ҩҵ�ɷ�����˾��ɽ��ʡ����ҽҩ�ɷ�����˾������ʡ���Ͼ�ҽҩ�ɷ�����˾���㶫ʡ�Ĺ���ҽҩ����˾��ҩ����һ��ҩҵ�ɷ�����˾�ȡ�
����Ŀǰ������ҽ�����ߵ��ƽ�����ҵ����ѹ���Ӵ������Ե�ҽҩ��ͨ��ҵ��ʼ�����ϵ���ҽҩ��ͨ��Դ���Ӵ������³����ȣ�����������������
�������忴��������ҽ�����ߵIJ����ƽ�����ҵ�ڼ沢��������Ϊ��̬��Ŀǰȫ���Ѿ��γ��ļ�ȫ������ͷ�Ͷ����������ͷ��ҵΪ��ֵ���ҵ��̬��
��������ǰ�ļ��ڹ�ģ������Ӫ�����罨�衢����ҩƷ�����οͻ���Դ�Ŀ�����������������������ͷ��ҵ�о����Բ�࣬��������ͷ�����ں��Ѹϳ��ļ�ȫ������ͷ��ҵ��δ��“4+N”ģʽ����Ϊ��ҵ������֡�
����Ϣ��Դ�������о����棩Top
������ҽ�ĵ�ȫ�����У���CFDA������ϡ�ҽԺ�طѡ�ҽ��֧���ĸ��Ʊ����صȸ��ִ������֮�£��в�������Ϊ��“ҽҩ��ҵ�����ӣ�Խ��Խ���ù���”��
������������һ�䣺������̫�ѣ����ǹ�ȥ̫���ף�2018�꣬ҽҩ��ҵ���ø���������
�����������������
�����ݺ�֤ͨȯ������2017��A��ҽҩ��ҵ��˾�Ѿ���ҵ���Ϸ�ӳ����ӳɡ���Ʊ�Ƽ��б꽵�۴����ĸ���Ӱ�죬Ԥ��2018���°�����ֹյ㡣
����1����Ʊ��ʹ��ҵ���ټ���
��������2018��1�£���Ʊ���Ѿ���ȫ��24��ʡ��ִ�У���½����7��ʡ�ݾ����ڹ����ڣ���֤ͨȯԤ�ƣ�2018��ף���½31��ʡ�ݽ�ȫ��ִ����Ʊ�ơ�
�����ڹ�����С����ͨ��ҵȥ��棬ͬʱС����ͨ��ҵԭ��Ʒ����Ȼ��ҽԺ���ۣ����´�����ͨ��ҵ��������ͬʱ����ҵ��û�м������ӡ���ˣ���Ʊ�Ƴ��ڣ��Դ�����ͨ��ҵ��Ӱ���Ϊ����Ӱ�졣
������Ʊ����ʽִ�к�С����ͨ��ҵ����ҩƷ�˳�ҽԺ��������ͨ��ҵ�û���հף���ͨ��ҵ���ж���������������
����2����ӳɵĸ���Ӱ��������
��������2017��ף���½31��ʡ����ȫ����ɹ���ҽԺ��ӳɸĸ��ӳɶ���ҵӰ��ּ���������������ҩƷ��ͨ��ҵ���ָ�����������
������֤ͨȯ��Ϊ����ӳɵ���ҽԺ��ҩ�������٣�����ҩռ�ȿ����븨����ҩ���ƣ�ҽԺ��ҩ����ҩ������ٻ��ж����»���������ҽ������ij�������������ҩƷ���ٽ��ָ�����������
����3���б��Ӱ����С
����2015�����Ժ7���ĺ�����ί70����Ҫ���ʡ��2015�꿪����һ���б꣬����2017��ף�27��ʡ���Ѿ�ִ���±ꡣ
��������2015����һ���б�ɱ�ۣ�δ������ҩ�б꽵�۷��������Ż���ͬʱ��ҽ��֧���۸ĸ��һ��������������ʹ��Ʒ�ʷ���ҩ��ռ����������Ʒ�ʷ���ҩ���˳��г���������ͬ��ҩƷƽ���۸�ָ�����ˮƽ��δ���б����ͨ��ҵӰ�콫Խ��ԽС��
���������������
���������꣬����Ϊҽҩ��ҵ“�ؼ�֮��”�����룬�ж��ٸ��ط���ҽҩ��ҵ��Ϊ�ʽ������⡢˰Ʊ���⡢���������ͣҵ���ٵġ����沢�ģ�����ֱ�Ӳ�����……
������ͳ�ƣ�ȫ��1.19�����ҵ������2017�����ʧ��1050��ҡ���ר��Ԥ�⣬��δ��һ��ʱ��֮�ڣ�����50%�����������ҵ������ʧ��
�������“Ӫ����”“��Ʊ��”�Ѿ���أ�ҽҩ��ͨ��ҵ�������ع��ѳ���ʵ����ϴ�����ڽ��С�
��������ǰ���ܶ�ҽҩ��ҵ������Ʒ���Ӽ������еĻ����ҳ��֣�������Ϊ���κܶ��ն���Ϊ�������淶������Ҫ“Ʊ”�����ܶ��ҩƷ�����̶�“Ʊ”�������Ϊ��ʢ��
�������ԣ�����ҽҩ��ҵ���ԣ���ҩ��Ǯ�Ѳ���Ҫ��“Ʊ”Ǯ���У�������ͨ��ҵ����“����”���ֿ���֧���жһ�Ʊ�����Լ�ʹ��С����ҵ��˾��Ҳ���Ա����ʽ�ķ��ա�
�������ڣ��йز��Ŷ������ն˵ļ�ܸ����ϸ���ҵƱ�ݹ�������Ҳ���ϸ�����Ʊ�ĸ��廧Խ��Խ�٣����յ�������“������”�Ŀݽߡ�δ����ʣ�µ�ҽҩ��ҵ���ܻ���Ϊ���¼�ֵ������——�ն�����ְ�ܡ���ҵ���ְ�ܡ�
�������⣬ҽҩ��ҵ�ǿ�“����”���ܶ�����ľ�ͷ�����������أ�
������ҽҩ��ͨ����˳�ᡢEMS�ȵ�����������ͷ�Ѿ�ɱ�����ˣ�δ���������ĵ������������룬������������ֲ���������������ռ�кܴ�����ƣ�Զ�Ǵ�ͳҽҩ�����ܱȣ���Ҳ����ҽҩ��ͨ�г�����ʮ�־�ij����
������Ȼ�����ڵ�ҽҩ��ҵ�Dz�����ǰ�����ˣ����ǣ�������û�и���ѡ�������£�����������������Ӧ�ı�������������������ɵģ���Ȼ��ҽҩ��ҵ��ٮٮ�ߣ�
����Ϣ��Դ����������Top
2��26�գ����Ϻ���һ����ҩҵ(����)�ɷ�����˾����2017���ҵ���챨��ҵ���챨ָ����2017���һ����ʵ��Ӫҵ������7,751,139,413.84Ԫ��ͬ������24.03%�������ܶ�ߴ�490,110,001.61Ԫ��ͬ������19.72%�����������й�˾�ɶ��ľ�����Ϊ400,753,399.10Ԫ��ͬ������13.41%��
����Ϣ��Դ��21����ҩ�꣩Top
2��26�գ������Ƿ�������Ʒ�ɷ�����˾����2017���ҵ���챨����˾2017��Ӫ��Ϊ13.43��Ԫ��ͬ������201%������Ϊ4.32��Ԫ��ͬ������1229%�����������й�˾�ɶ���ÿ�ɾ��ʲ�1.84Ԫ��ͬ������16.46%��
����ҵ���������Ƚϴ��ԭ����������ʾ���������ڣ�����2016��“3.18������ҵ�¼�”��������ҵ���߱仯�Ȳ�ȷ��������������������ҵ�����������ʵʩ����ҵ�����õ���һ���淶�뾻������˾������Ʒ�������Ķ��������Ʒ�ƹ㼰���۵ȹ���½���ָ���
����Ϣ��Դ������ҽҩ��Top
�ֹܾ�����ע��88��ҽ����е��Ʒ���棨2018���24�ţ�2��27�շ�����
2018��1�£�����ʳƷҩƷ�ල�����ֹܾ���ע��ҽ����е��Ʒ88�������У����ڵ�����ҽ����е��Ʒ37�������ڵ�����ҽ����е��Ʒ20�������ڵڶ���ҽ����е��Ʒ31����
����Ϣ��Դ������ʳƷҩƷ�ල�����ܾ֣�Top
�ټ�������һ�Ҵ�����ҵ���ε�����ҽҩ��˾��רע�����ڰ�֢���ƵĴ����ͷ��Ӱ������������ҩ��Ŀ�������ҵ������˾������������®�����ǶȰ�������й�ʳƷҩƷ�ල�����֣�CFDA������������ɺ��ã����ƴ�ǰδ�������Ҳ��ʺϽ�����ֲ�Ķ�Թ�������MM�����껼�ߡ�������һ�ֿڷ����ߵ���ҩ���2013���״����й����CFDA����������ɺ��ã����������ܹ�����һ���Ʒ���MM�ij��껼�ߡ��ټ����ݻ���»���˾��Celgene������Ķ��Ҿ����������й��������۸�ҩƷ��
����Ϣ��Դ����ͨ�磩Top
Top
2��26�գ�������ҩ�ƣ�����FDA����abemaciclib���Ϸ��㻯ø���Ƽ���Ϊ���ƾ��������������ԡ��˱�Ƥ������������2-�������ڻ�ת�������ٰ�Ů�Ի��ߵij�ʼ�ڷ����Ʒ���
����Ϣ��Դ������ҽҩ��Top
2��26�գ�������ó�������Ƽ��ɷ�����˾��������ƣ���˾�����з���������˨��ҩ“ע������������֯������øԭ������Ĺ��壨rhM-tPA��”����Ʒ��������ͨ��������ҩ��ίԱ�������˶�ͨ����Ϊ“ע����������ø”����˾��2018��1��18�������ʳƷҩƷ�ල�����ܾ��ύ��“ע����������ø”����ҩ�������룬����2018��2��23����ʽ�õ�����֪ͨ�顣
����Ϣ��Դ������ҽҩ��Top
�������Խ����Լ��������������ҩ���ձ�ҩ��Э�������Ultragenyx�����ĵ���Burosumab������ŷ�˵�����������
��������X��������Ѫ֢��XLH���ĵ�һ�����������ҩ��
Burosumab���Խ��XLH�е���άϸ����������23��FGF23���Ļ��ԣ���������1���Լ�1�����ϵĶ�ͯʹ�á������������������ΪCrysvita��
����Ϣ��Դ��������ihealth��Top
KemPharm��������������FDA����Apadaz™����ҩ���루NDA����Apadaz™���������ƶ��ڣ�������14�죩�����ض���ʹ����Ҫ�ð�Ƭ��ֹʹҩ����û���ʵ�������Ʒ�����Apadaz��KemPharm��ǰ��ҩ��benzhydrocodone�Ͷ����������ӣ�acetaminophen��APAP���������ͷţ�IR����ϣ���FDA������Hydrocodone/Acetaminophen��ǰ��ҩ�
����Ϣ��Դ��ҩ�����£�Top
�ܲ�λ����ʿ��ObsEva SA����һ���ٴ��ε�������ҩ��˾��רע��15��49��֮�仼����ֳ�����ͻ����ϰ��ĸ�Ů�����Ʒ��Ŀ�������ҵ����2��27�գ���˾����������������ܾ����������ʵ���ҩ“nolasiban”�����ٴ�����ȡ���˻����Ķ��߳ɹ���
����Ϣ��Դ������̽����Top
���ڣ�һ�����pimavanserin���ư��Ⱥ�Ĭ�����߾���֢״��˫ä��������2���ٴ�����Ľ��������3�·ݵġ�Lancet Neurology����־�ϣ����о���Ӣ���������ش�ѧҽѧԺ��University of Exeter Medical School����Clive Ballard��ʿ�쵼��
Pimavanserin��һ��ѡ����Ѫ���ط�������SSIA���������Ȱ���5-HT2A���壬��Щ������ʧ��֢��صľ����з�������Ҫ���á�Ŀǰ��Pimavanserin���ڹ㷺���ٴ���Ŀ�н����������漰������Ӧ֢��2016�꣬FDA��Pimavanserin��NUPLAZID®����������������ɭ���йصĻþ������룬�������ڸ���Ӧ֢��ҩ�
�����о��Ľ����ȥ����еİ��Ⱥ�Ĭ���ٴ����飨CTAD�������Ϲ����������ʾ���ڵ�6��ʱ���������NPI-NH�����½�39.5%�����Ը��ڰ�ο�����19.3%���ﵽ���о�����Ҫ�յ㡣���ң�û�й۲쵽pimavanserin�Ի��ߵ���֪������
����Ϣ��Դ��ҩ�����£�Top
2��22�գ���������˹��������FDA��������Դ��PD-L1����¡����MSB2311�������ƾֲ����ڻ�ת����ʵ���������ٴ��������롣����˹�����ѿ�ʼ����MSB2311���״ν������壬�����ԡ������ġ�������������չ���ٴ��о���MSB2311������˹�����һ�������ٴ������ε��������ӡ��ݳƣ���FDA������PD-L1������ȣ�MSB2311�������ж��صĿ�ԭ��ϱ�λ�������뿹ԭPD-L1�Ľ���ж��ص�pH�����ԣ�������MSB2311������������֯�л��գ�����������
����Ϣ��Դ��ҩ�����£�Top
Kadmon��˾����������һ�����ڽ����е�2���ٴ�����Ķ��߽���������о�ּ�������ù�˾��ROCK2��Rho-associated coiled-coil kinase 2����ø���Ƽ�KD025���ط��Է���ά����idiopathic pulmonary fibrosis��IPF�������е���Ч�Ͱ�ȫ�ԡ���ЩIPF����֮ǰʹ�ù������ṩ����������ͪ��pirfenidone����/��nintedanib���ơ�������ʾKD025�����������ã������ֳ��ٴ��洦���ڵ�24��ʱ���ߵ������λ�����FVC����ƽ���½���Ϊ48���������������֧�����ƣ�BSC�����ߵ�ƽ���½���Ϊ175���������Բ�ֵΪ127��������Բ���Ϊ73%��
����Ϣ��Դ��ҩ�����£�Top
Mesoblast��˾����������������̴������Լ�����ֲ���������aGVHD����������������ʸ�ϸ����ѡ��ƷMSC-100-IV��remestemcel-L����3���ٴ������ڵ�28����ܻ����ʣ�ORR����ȫ����+���ֻ��⣩�ɹ��ﵽ��Ҫ�ٴ��յ㡣
����Ϣ��Դ��ҩ�����£�Top
2��26�գ���̨��������Ƽ��ɷ�����˾����������֯����Ĥ�ٴ������չ����ƣ������鷽����Ԥ��Ŀ�����ٴ������Ч������ƫ�룬������ֹ“��֯����Ĥ”��Ŀ��
����Ϣ��Դ������ҽҩ��Top
���գ��й��������Ź��ں������ˡ����СС��“+”�ţ�����ԺΪ�ν������š�һ�ģ���һ�����������ǣ�������+��ҵ���¡�+�Ƚ����졢+ҽ�ơ�+ʳƷҩƷ���……“����ҵ�����뻥��������ںϡ�”“������+”�ѳ�Ϊ������ᴴ�·�չ����Ҫ����������ҽҩ��ͨҲ�����⡣
����“������+ҽҩ��ͨ”���������Ǽļ����ϵı�Ҳ��������Ϊ���û�����������ȥ�������������ͨ������������ҽҩ��ͨ���������ںϣ���ʵ��ҩƷ��ͨģʽ��ת�����������û���������Ϣ�����������ⲿ������Ϣ���ڲ������������ϣ�ʹ��ҵ��ҩƷ�������������͡�ҽҩ���̵ȷ���ʵ�ָ�Ч�ʲ������ٽ���ҵ����
����“������+ҽҩ����”����ʹ��ͳҽҩ��ҵ�ܹ����û������������������ռ����洢���������Ƽ���ȣ��Ӷ��ؿ���ͨ·����ʵ�ָ�Ч�����ϡ�������ҽҩƽ̨��ͨ��ʵ������ҽҩ��ҵ�������̡���Ӧ�������βɹ��̽�����Ϣ����Խӣ������µ�ҩƷ���ڰᵽ���ϣ�������ͨ���ڣ����ͳɱ���
������“������+”�µ�ҽҩ��������
����“������+ҽҩ����”�����ڻ���������֧�����˴����ݵ�����ָ��ϵͳ�������������ֳ��ն��豸���ռ������ƶ�����������Ϊ������APPʹ����ҵ���ø��ӱ�ݡ�ʵʱ�����۹����⣬���������̵ķ�չ�����ҽҩ������ֵ�����������Ӱ�죺
����һ�Ǵٽ��������������������߹�ҩ������������С�Լ���ɢ�����أ������ɱ�����̧�ߡ�����ʵ��������ҽҩ��ҵ���ԣ�ѡ��������������ڰ�����õİ취������������ҵί�е�������������ҩ�������ҵ�ɳ��ƹ���ҽҩ����ϵͳ���ﵽGSP��ϵҪ����ҽҩ���̹�Ӧ�������ӣ��ٽ�����������������
�������ǵ�������������Ϊ������ֵ���������£��ƶ���Ϣ�����������Զ��������̻���
��������Ժ�칫��ӡ�������ڽ�һ���ĸ�����ҩƷ������ͨʹ�����ߵ�����������У���������ҩƷ�ִ���������Դ��ʵ�ֶ��Эͬ��֧��ҩƷ��ͨ��ҵ���������ͣ��ӿ��γ��Դ��Ǹ���ҵΪ���塢��С����ҵΪ����ij���ҩƷ��ͨ���硣ͬʱ��“��Ʊ��”��ʵʩ�����ѹ��ҩƷ��ͨ���ڣ�����ҩƷ���ۡ�������������ҵ�ļ�Լ������Ϣ�����������̡��������֣�2017����ҳ�̨�漰ҽҩ���̵���Ҫ���߷����֪ͨ���٣��������ذ�����δ��ҽҩ���̷�չӰ�����ĵ���ҽҩ����“��֤”��ȡ�������Ž��ͣ��ƶ�ҽҩ�������硣��Ȼ����Ȼ����ȡ���ˡ��ż������ˣ����Ҳ�����ϸ��ˡ�
����������֪���ոչ�ȥ��2017�����ϲ��꣬����ҩ��ͦ��ȥ�ˣ����ڻ��������ó���£���Сҩ���Ƿ������������Ǹ�δ֪��������Ͱ͡������̳ǡ���èҽҩ�ݡ�1�ŵꡢ˳��ȿ�绥������ҵ�ݷֺ�����ҽҩ������������ҵ��ҽҩ������ҵ��ת�����������Ӹ���Ч�����á�
���������ٷ�������ʾ������2017��6�£����������Ѹ���ȫ��2691�����أ���Ӫ��������99%���˿ڡ�52%�Ķ���6Сʱ�ʹ92%�Ķ������մ����մ���ͬʱ������������2017���°����Ƴ�“ҽҩ�Ʋ�”��Ŀ��ּ��Ϊ�������ṩ����ϵͳ����ҽҩ��Ӧ����������������˲ִ������䡢���͵ȸ����ڡ������Ŀͨ����˵����ҩƷ������ҵ����Ʒ��ǰ����ҽҩ�Ʋ֣������ն˿ͻ��µ����ɾ��������������͡�
��������չʹ���Դ�
����“������+”��Ȼ�Ѿ���Ϊ�������ҽҩ��ͨ��ҵЧ�ʵ��¡��ɱ��ȸ߱˵���������һЩ������ij���Ҳ��Ӱ����ͨ���ơ�
����1.�����������IJ�ƥ�䡣����ҽҩ��ҵ��������ͳ��ҵ��Ƚ϶��ԣ����г����ŵ���Խ���������ҽҩ������������չ��ģ���������ij��֣�����ͬ�̶ȵ�Ϊ�г��ķ�չ���˺��ȡ�����ѡ��������ҩʱ�����н�Ϊ���ȵ�ʱ��������OTCҩƷ��ҽ����е������Ҫ�����װ������������ʩ����ҽҩ������������˸���Ҫ����������Ӫ������ҽҩ������ҵ����רҵ��������ҽҩ��ͨ��ҵ�����������������ȷ����ƷƷ�ʣ���δ�õ���������
����2.����ϵ�����ͺ�������ҽҩ�����������ʵͣ�ijЩ���������յش���һЩҽҩ��������ޱ��������������������ͳһ��ȱ����ҵͨ�ñ����ٴΣ�������ҵ��ģ��һ�����൱һ������ҵ�Ա�������û����ʶ����ʶ���㣬���ڳɱ����صȵĿ��ǣ�ȱ��ִ����ر����Ծ��ԡ�
����3.ҽҩ�����������ӡ��ڵ��̡��������ͻ������ķ�չ�����£������ߵ�����Խ��Խ���Ի���ҽҩ����������������Ƭ������ʱ��С�����������ε��������������ԡ��ҹ�ҽҩ��Ʒ��Ӧ���ڵ�϶࣬��ͨ�����뽻���ӡ�ҩƷ����ͨ�����ϵļ��Ҳ������һЩ�����������ۺ�������ⲻ�ܼ�ʱ����������˷��˴����������Դ�����ջ�����ҽҩ�۸����ߡ�“������”��������⣬���봴��ҽҩ����ģʽ��
�������ƾ�֮��
����ҽҩ����δ����չ������������Χ��“������+”�����ϴ��£�����“������+ҽҩ����”���ں��Ʊؼӿ�ҽҩ������Ϣ�����裬������Դ���ϣ�����ҽҩ������Ӫ�ɱ����������������ҵ����������
����1.����ն�����ģʽ������������������͵��ն˻��ߵ�����ҽҩ�����ն�����ģʽ����DZ�Ȼ��ҽҩ������ҵ��ҽҩ��ͨ��ҵͨ����Ӫ��רҵ������ҽҩ�����ķ�ʽ��������������͵��������ն�������ϵ���������͵��ŵꡢ�ŵ����͵��ҡ�ֱ�����͵��ҡ����͵�����ȡ���㡢ȡҩ��ȣ���
�������ƶ������������ƶ��£��ն�������ϵ����ͬ���з��û�����ȸߵ���Ϣϵͳ��������ն�APPӦ�ã��ɰ���ҩƷǩ�ա��ص�ȷ�ϡ��쳣ҩ��ش���������ҩ���ѡ���ҩ���̲�ѯ�ȶ��ֹ�����ϣ���
�������⣬��ν���ն��������һ����������ǽ�����̽�����ġ������п��ֱ�ͣ��������������������ǰ���֡�ͬ�����ͣ������������������������ʽ������̽���������ֿ����������ۻ��ܣ�Ԥ��ҽҩ�������ն����;�����ȫ����졣ͬʱ����������ػ�����ʩ��Ҳ��Ӵ�Ͷ�룬�������ļ�����չ�߶����������������ʩ��������ҵ��صķ���ҵ�����ҵ������ҵ�ȵIJ������ƣ���Ӫ�����õ�����������
����2.������������ҽҩ����ȫ��λ�ܿ�ģʽ��ҽҩ������ҵӦ���ڴ��¸ĸƽ̨���ϡ����˺�����ȫ���Ž���ȷ������ط��������ȣ����Ҳ����ϸ����ҩƷ�������ѿ�ҩƷԴͷ����Σ���ҵͨ�����Ӽ��ϵͳ�ϴ�ҩƷ������Ϣ��ʹ�������ܼ����ҩƷ������������������̶�����ϵͳ���֮�£�����“ҩƷ����-ҩƷ��ͨ-�û�”��ȫ�̼����ϵ���ڴ���Ҫǿ�����ǣ�ȫ���ҩƷ����ϵ���轫Ϊ������ҽҩ���۳�Զ�������ķ�չ�춨���������淶����ҩƷ����Ч��ֹ��ðα�ӣ�Ҳ����ҩƷ��ͨ���̳�������ʱ��ʱ��������ڣ�����ʱ��ȡ��ʩ��������ҽҩ������ҵ�Ĺ�ģ������Լ����
����3.�ƽ��������衣��ǿ��ҽҩ��������������о���Ϊ�ӿ��ҹ�ҽҩ���������������ƽ�ҽҩ�����������̵춨���ۻ������ƶ����ҽҩ�����Ļ������������������ҽҩ������ҵ���ż���ҽҩ������ҵ��Աְҵ����Ҫ��ҩƷ��������淶��ҩƷ��������װ������Ȼ����Ա����й淶����ȷ��ҵ��Ա���ʡ�ҽҩ�ִ������价����ҵ�淶�ȡ���ǿ�����������������������ҵ��ҽҩ��������Ҫ�Ե���ʶ��������ҵ����ҵЭ��ȴ���������ʵ�ʳ������������ʵ��Ҫ���ҽҩ�����������Ҫ����ע��רҵ�˲Ŷ���������뽨�衣
����4.ʵ����Ч�������ƶ��������ܹ�����ҽԺ��ҽҩ��ҵ�ȸ�����������Ҫ��ͬʱʵ����Ϣ������������������Ч�ʡ�ҽҩ������Ҫ���ƶ����������н�ϣ�ȥ��һЩ�м价�ڣ���ֱ�ӵض���Ϣ���д��ݡ������������������ģ���ҽҩ������ҵ������һ��APP�նˣ�ʹ��ҽҩ��ҵ��ҽԺ�ܹ��������APP��ʵ�������µ��Ĺ��ܡ�Ҳ���������APP�����в���ҩƷ��棬��������Ϣ���и����˽⣬��ʵ��ȫƷ��ȫ����ȫ�̿��ӻ������ݣ�����ʵ�����������ӡ���������ʵʱ��ء�����ѧԤ�⼰���ߡ���Ӧ����ЧЭͬ�ȹ��ܡ�
������ͳ��ҽҩ��ͨ����������㣬“������+ҽҩ����”�ջ�ʱ���ĵ�������ʱ�գ������ҵ���кܶ����Ҫ���ơ���������֧�����ȵIJ��ϼӴ�������Ͷ������ӡ���ط��ɷ�������ƣ���ͳҽҩ��ͨ�뻥���������и��õ��ںϡ������Ƚ��������豸����Ϣ����������������������ϵͳ���б�Ҫ�����ϣ�ʵ��������Ϣ�Ĺ����ͶԽӣ�����ʱ�����ٻ���ֻ�����������ܸ��õؽ���ҽҩ����ijɱ����������Ч�ʣ������ҵ��������Ҫ��
����Ϣ��Դ��ҽҩ���ñ���Top
���ڹ��ڷ�Сϸ���ΰ��г����ԣ����;������ҵ�����ɱ���ƣ���Ҫ�������е�ʱ���ˡ����ڰ�˹�����й�����һ�����һ������ԣ�̩��ɳ��˳����ֻ����Ļ��̩��ɳ���й���������ҩ���е��ٶ��¼�¼��
����̩��ɳ���й���������ҩ���е��ٶ��¼�¼��
�������ڰ�˹�����й�����һ�����һ������ԣ�̩��ɳ��˳����ֻ����Ļ�����ڹ��ڷ�Сϸ���ΰ��г����ԣ����;������ҵ�����ɱ���ƣ���Ҫ�������е�ʱ���ˡ�
����3��24�գ���˹������������ʳƷҩƷ�ල�����֣�CFDA�����������ΰ���������ҩ��̩��ɳ�������������Ƭ�����й����С��ⲻ����ȫ���һ�����еĵ������ڷ����������ѡ����EGFRͻ�����Ƽ���Ҳ���й�������������EGFRT790Mͻ�������Եľֲ����ڻ�ת���Է�Сϸ���ΰ�ҩ��������Ǵ�����2007�껯ҩע�����ʵʩ�����ҩ���й����е��ٶȼ�¼��
����2015��ף�CFDA���������ڽ��ҩƷע�������ѹʵ�����������������������������壩����������ɫͨ�����ӿ��ٴ������ҩƷ������������̩��ɳ��˵���ӽ�����ɫͨ������ʽ������ֻ�����߸��µ�ʱ�䣬����ʱ����������������Ҳ����ֻ��16���¡�
����������Ԥ��
����2015��ף�CFDA��̨ҩƷ���������������ߣ�������ǽ��ҩƷע�������ѹ��ijЩ�ٴ����衢�г���ȱ��ҩƷע�������Ŷӵ����⡣
����ҩƷ�������ٶȶ���ҩ�����Ҫ�Բ��Զ�����������ҵ��˵�����������ƶȼ�������ҩ�ŶӵȺ��ʱ�䣬�������ҩ�з���Ч�ʣ��ӿ���ҩ���У�������ҵ��˵�����������ƶ�ʹ����������Դ���º��ٴ�����Ʒ����б����ҵƷ����Ʋ��ӵľ�����õ����⡣
�����ڽ��������ڼ�IJ���ͨ���ϣ�CFDA�ֳ��Ͼ�Ȫ�ڻ�Ӧ“���ֹ���ҩ������”������ʱ��ʾ����������ȷʵ���ڣ���ԭ���Ƕ��ģ������ƶ���ơ�֪ʶ��Ȩ��������δ��ʵ��ҽ��Ŀ¼��������ʱ�Լ�ҩƷ����Ч�ʵȡ�
����һֱ�������������������߳���һ���ҩ���й���������Ҫ���������������ͺ�6�굽8���������á������������ƶȵĽ���������һ������ҩ���ٴ�����ҩ��������У�����һ��“ȫ����”ҩ��������ٴ���
��������Ŀǰ������ʳƷҩƷ�ල������ҩƷ�������ģ�CDE���ۼƹ�ʾ25��������������������ҩƷ������271��ҩƷ��������������ɫͨ����
����“ʵ���������ڽӵ�CFDA����֪ͨ��ʱ���ڲ��Ŷ����̩��ɳ�IJ�Ʒ��ѵ����û����ɡ�”��̩��ɳ�й����з������ϣ���˹�����й����ܲá�����ҵ����������̹�ԣ�̩��ɳ�����ٶ�֮����ȫ���������ǵ�Ԥ�ϡ�
����̩��ɳ���й��Ļ������У���������ʽ�ύע�����벻����������ҵ�ʱ�䣬��������ʽ�ύ�������벻�������£���2015��11�»������FDA��Ҳֻ����6�������ҡ�����¶��̩��ɳ�й�����ʱ��滮������������ȫ��CEO�������ϣ��ɴ˿ɼ���˹��������̩��ɳ�й����еĸ߶����ӡ�
������Ϊȫ���һ�����еĵ������ڷ�����ҩ��̩��ɳҲ���й�������������T790Mͻ�������Եľֲ����ڻ�ת���Է�Сϸ���ΰ�������ҩ�����Ŀǰ���й�û��ͬ���Ʒ������Ӧ�������ݻ��FDA���������У�����������������ʾ��̩��ɳ��Ϊ�����Ʒ�����Ⱥ�����ҩ��Ķ��������ƿ�ʹ��չ�����������ӳ�5.7���£���Ҳ�����ܹ����������ھ��ܽ����������ͨ����ԭ�����ڡ�
������˹�����й����ܲá���ҵ�������г��븺���˻Ʊ���Ϊ��ͨ��̩��ɳ�Ļ�������������ҩ����ϵ�ĸ�Ч��ת���Ժ�Ҳ���ܻ�������Ʒ�ֵĿ��ٻ���������һ���棬�����������Ʊ����������㣬Ҳ�����������ĸ�Ч�ɹ����Ѹ��Ƶ�����Ʒ�֡�
����������ɱ
������������ͳ�ƣ�2015���ҹ����ڷΰ��г���С���Ӱ���ҩ���г���ģΪ32.3��Ԫ��2010�ꡫ2015�긴��������Ϊ22.6%��Ŀǰ��Ҫ�����ֲ�Ʒ�������ᣨ�����ɣ����������ᣨ����ɳ���Ͷ������ᣨ�����������������ƽ��ܹ����ƻ����ڻ��Ƶľֲ����ڻ�ת���Է�Сϸ���ΰ���
����̩��ɳ�����У��ð�˹������֮����������������һ������������ͳ�ƣ��й���Сϸ���ΰ���������Լռ�ΰ�����������80%-85%��Լ����֮���Ļ����ڷ�ҩ1�����һ�����T790Mͻ�������ҩ����̩��ɳ��Ŀǰ���T790M��ҩΨһ��ҩ��ѡ��
������Ϊ��Сϸ���ΰ��г��ϵı���ѡ�֣�����ҩҵ�Ŀ������ڳɹ���Χ��������ҩ��̸��Ʒ�ֺ�ͨ������54%��2016��ʵ��Ӫ��10.35��Ԫ��ͬ������13.36%������ͬ������31.46%���ò�ƷҲռ������ҩҵ��Ӫ�յ�99.98%����������2017���°�ҽ��Ŀ¼��Ҳ��������δ�������ɵ��г����ۡ�
������һ�ҿ��ҩ�����ϣ�������ѡ����������ҩ��̸��Ʒ�֣��������ڽ���ɹ���Χ�ڶ��ֹ���ҩ��̸�У����۷��ȳ�����50%��
�������⣬2017��3�£����ָ����������ȫ�����Լ�ĿǰΨһ���еĵڶ�����������TKI�ࣨ�Ұ��ἤø���Ƽ�������ҩ�ﰢ�����Ὣ��ʽ��½�й��г�����������Ŀǰ����70������ұ�����������EGFRͻ�����Է�Сϸ���ΰ����ߣ����ڶ�����ҳ�Ϊ��EGFR����ҩ�����ѡ��
��������ɳ��2005�����й������𣬾�һֱ���й�EGFR-TKI�г��ݶ���ߵ�ҩƷ�������н��б�������ʾ��2015�꼪���������й����۶�Ϊ12.43��Ԫ��Լռ�й�EGFR-TKI�г��ݶ��38.5%�������ű�����ҵ���������ҩ���ǿ�ƽ��룬��˹������ƾ������ɳ�ڹ��ڷ�Сϸ���ΰ��г���ǰ�н��������ѡ�
������̩��ɳ�Ļ������ھ������漤�ҵĵ��¸��˰�˹����һ����Ҫ�������ܹ�������ڵ������е�������Ʒ̩��ɳ���Ӿ������ĽǶ���˵�������ܹ�����ס���µ��г��ݶ���һ����㹻��ʵ��������Ϸ��������
������һ�����ܹ�ע��������Ǽ۸�����Ŀǰ̩��ɳ��û�н���ҽԺ����˹���;����Ҫ����ҩ�������˽⣬̩��ɳ�ļ۸���ÿ��5��Ԫ���ҡ�������̩��ɳ����Ԯ����Ŀ�����粡ǰ�ͱ����߽���ѻ��ҩƷԮ��ֱ��������չ�����ǵͱ����߿���ʹ��̩��ɳ4���º�������룬��������һ�����ɻ��8���µ�Ԯ��ҩƷ���˺�������ʹ��̩��ɳ3���£����������Ļ����ɼ�������Ԯ��ֱ�������չ��
����������Щ�Ѿ����еIJ�Ʒ�⣬�����������ŷΰ������ʵIJ������ߣ�������ҵ�ڸ���������ҩ�г�����Ҳ�ڲ������ӣ����Ӵ�Կ�����ҩ�����Ͷ�롣
����Ŀǰ������������25�ҹ�˾�����뼪������ķ��ƣ�����28�ҹ�˾�������������ķ��ƣ��������в�������ҽҩ������ҩҵ������ҩҵ��ʵ��ǿ������ҵ�������С�2016��ף���³��ҩ�з��ļ���������ҩ����ɾ�CFDA��ȡ���������ɳ������ĺţ���Ϊ�й���ҩƷ�������ɳ������ƶ��Ե�Ʒ�֣�����2017��2����ʽ���С������˹�ע��������ɵ�����ֱ��ʹ��ԭ�в�Ʒ����ɯ�ļ۸�ÿ��5000��Ԫֱ����2000��Ԫ��
����Ϣ��Դ��Eҩ�����ˣ�Top
�ݹ�����2017�꣬�����й�����ҩ��ҵ��������ն��38��ANDA�����ĺţ����а���31����ʽ�ĺš�7����ʱ�����ĺš������������Լ�һ�������۵����ߵ�����֮�£�������֤Ʒ�ֵĹ��ڼ�ֵ�������ԡ��Ƽ����ʻ����������ͬʱ��ANDA�Ļ���Ҳ�ڸ���̶���Ϊ��ҵ���������������г��Ļ�������Ȩ��
���������2016��8���й���ҩ��ҵ�������ջ�22��ANDA�������ԣ�2017��31��ANDA��ʽ�ĺš�7����ʱ�����ĺŵ�ս�����ƺ����������й���ҩ���Ž��������г���ˮƽ���ָ�һ�
��������������2017��������ȡ��ANDA��ʽ���ĺŵ���Ȼ�ǰ˼ҹ�˾�����ջ��������ɶ����٣������ǻ�������˹ͨ��8���������պ���6������ʯҩŷ�⣨5����������ҩҵ��4�������˸�ҩҵ��3��������ͨ���ǣ�3�������Ϻ���������1��������Ʒҩҵ��1������
������ȡ����ʱ�����ĺŵ���ӿ�ֳ�һЩ������ף���������ҩ����Ե�������Ƿǡ�������̩���������˫�ҡ�����ҩҵ����ɳ̹�ⰱ����Լ����貽��ҩҵ���������ǡ�
����������ҩҵ���ȾӰ���
�����������ϰ���ҵ�У�һ�����ȵ���Ȼ�ǻ���ҩҵ����Ϊ������ͨ��FDA��֤���Ƽ���ҵ�Լ��õ�������֤�����Ƽ���ҵ֮һ������ҩҵ���������Ƽ������Լ����ʻ���չ����ٲȻ�Ѿ�������Լ����������������й�˾����ͳ�ƣ���2007����������2009��һ����ֿյ�֮�⣬ÿ�껪��ҩҵ������Ӧ��Ʒ���������������������������������������ӵ�̬�ƣ�2016���乲��6��Ʒ�ֻ�������2017����ﵽ��ʷ��ߣ�������ʱ������������Ʒ������һ����10����Ʒ��2017�����ANDA��
��������������Щ��Ʒ�У���ֵ�ù�ע����2017��8�»�����������͡���ң������й���һ��ר����ս�ɹ���Ʒ�֡���ǰ�������ӹ�˾����˹ͨ��Actavis���ҹ�˾���ò�Ʒ��������͡���ҵ�ԭ�й�˾Noven�����ר����ս�����ջ���������ս�ɹ���
����Ҫ֪��������ڻ�����˵������һ������Ƿ������顣��Ҫ��Ϊһ������ҩ��ҵ��������һ���ܹ�������ר����ս��ϵ�����õ�ר��������ϵ��һ����������飬��Ϥ��Ŀǰ�����ϰٸ�����ҩ��Ŀ�����漰40��ר����ս��Ŀ����һ��ר����ս�ɹ������ɾ���ζ����ռ�г���������һ����ǿ��������͡���ҵijɹ�������֤������һ�㡣
����������һ��ֵ�ù�ע��������Ʒҩҵ�����ţ�������������ֶ�����Ƭ�����ҩ���ɻ�����������Ʒҩҵ��ͬͶ�ʡ���Ʒҩҵ�����Ʒ������Ʒ�֡��������������Ѷȸ��ߵĻ��ͼ����Ѿ���Ϊ�˻����ص㹥�˵ķ���Ŀǰ��2013������Ҳ����5�����ͼ��ͻ�����
����������֤ȯ���㣬����ҩҵ�˴λ�����11��Ʒ�֣���������Ʒҩҵ��ͬ������������ֶ�����Ƭ����2016���������г��������ܽ��Ϊ92.28����Ԫ���������ƽ��10%����ռ�ʲ��㣬�������ķ�ֵ���۽��ﵽ9.2��Ԫ��������ճ�����Ϊ�ն��ۼ۵�20%��������Ϊ15%���в��㣬��Ԥ�Ƹ���������12.0��Ԫ����������Ԥ��1.8��Ԫ������������
����������ҽҩ���������
������������ڻ���ҩҵ��˵������ҽҩ2017��6��ANDA�ƺ�����Ϊ���������ں���ҽҩ�������ԣ��������һ��������Ҫ֪������2011�����ҽҩ��һ��ANDA���������濵������ʼ���𣬵�2017��֮ǰ������ҽҩҲһ��ֻ��5��ANDA���������
������Ȼͬ��ǰ���ص�һ�����˴λ�����6��ANDA�У���5������ע������������ҽҩ�Ƽ����ʻ���ս���йأ�һֱ����������������ע����ȹ��ո��ӡ������ѶȽϸߵ������Լ��������������������г��������������ǰ������5��ADNA֮�У�Ҳ��3������ע�����Ҳ����˾���������Խ��٣�����������ҽҩ�����IJ�Ʒ�����ܴ�������������ذ���Ʒ��
�������ڹ��ʻ��봴�²��ص�ս��֮�£������г�Ҳ�Ѿ���Ϊ����Խ��Խ��Ҫ�ķ�չ����֮һ�������ǰ���ʾ������ӿ��ƽ������г�������δ��������ʹ��������Ʒ��ȫ��ͨ������FDA��ŷ����֤��Ϊ���غ����г��������
������ʯҩŷ�⣺Ծ������
����ʵ���ϣ����˻�������˹֮ͨ�⣬�˸�ҽҩ�Լ���ͨ���ǵij��ֶ�����Ϊ�档�Ѿ�˳������չ�����������ҩEpic�Ѿ���ʼΪ�˸�ҽҩ����ANDA�����˸��տ�2017��Ҳ˳����������ANDA���ġ���ͨ������Ϊʼ����ŷ���߶��г�Ϊ���ķ�ר��ҩ�з���������ҵ��������Ҳ��������FDA������Ϣ���ϣ�������ȥ���ڹ���Ҳ�в�����ҩ��������ƽ����Ƭ���������˫�ҿ���Ƭ��5��ҩ�����˳��ں������䷢չ̬��Ҳ�ɼ�һ�ߡ�
�������˾�ϲ����ʯҩŷ���ڹ�ȥһ��ANDA����ı��֡�����2016�꣬ʯҩŷ����Ѿ��������������˫��Ƭ��ANDA������CDE��2017��4��13�շ����ĵ�15���������������У���ҩ��Ȼ���У��䱻��������������������Ϊ“ͬһ�����ߣ������������У�����������еķ���ҩ”������ʱCDE�״��Դ����ɽ����Ʒ������������������������2017�꣬ʯҩŷ�������������ANDA�ĺţ����а����������������������г��������õ�Ʒ�֣�����ʯҩ���Ŷ��ԣ��������Ǹ�����Ϣ��
�����������Ƽ��ع����
�������ܶ�����ҩ��ҵ���ԣ��ܷ�ͨ��FDA��֤�Լ�ANDAƷ�������Ķ��٣��ںܴ�̶��ϴ�������ҵ�Ĺ����г���������Ӱ���������������������£����뿴����һ���ǣ�������֤Ʒ�ֵĹ��ڼ�ֵ�������ԣ�ʯҩ�����������˫��Ƭ��������������������һ�����͵����ӡ�
������������������ʵ������Ҫ�������㣬��Ҳ������ҵ�Ƽ����ʻ����������ͬʱ�������г����ɺ��ӵ�����·����һ�ǹ���ת��Ʒ�������������������ǹ��߲�Ʒ����ͨ��һ�������ۡ����Կ������ǣ�Ŀǰ�������߶����ں�������ĸ�����ANDAƷ�����ṩ��ȫ��λ��֧�֣���ע�ᵽ�б굽ҽ�����ṩ���������ߡ�
������ע���걨���棬Ŀǰ�Ѿ���ȷָ�����ں��������ANDA��Ʒ���Լ�һ��������������̣������ҩƷ������ҵ����ŷ�ˡ��������ձ������еķ���ҩ�����Թ���ע���걨���������Ϊ���������ջ�ѧҩƷ��ע������걨ҩƷ���У������к���ͬͨ��һ�������ۣ������й�������ͬһ��������������ŷ�ˡ��������ձ������еģ�����ͬͨ��һ�������ۡ�
���������ζ����Щ��Ʒ�����ڹ�����ҩѧ�о���BE���飬���ܽ�Լʱ�����ܼ����з�֧����һ����ԣ�ҩѧ+BE��Ҫһ��ʱ�䣬�з�֧������500����800��Ԫ���ң����һ����ҩ��ҵ������Ը�����ٶ�ͨ��һ�������ۣ���ռ�����г���
������Ȼ�Ի���ҩҵΪ�������걨��8��һ�������۲�Ʒ��2017��6��7�ջ�2017��7��31�ջ��ע��������9��25�ս����������ģ�7����Ʒ��12��27�ջ�����Ϊ����ͨ��һ�������۵Ĺ��ڷ���ҩ�������й�����ҩƷĿ¼������ע��������������6���µ�ʱ�䣬����������ʱ���3����ʱ�䡣�����6��ANDA��Ʒת������������ע�����룬����5��Ʒ�ֽ�������������
����������ͨ��һ������������ζ�Ų�Ʒ��δ�����г��б��н��õ�������ơ����յ��µ����ߣ�ͬƷ��ҩƷͨ��һ�������۵�������ҵ�ﵽ3�����ϵģ���������������ҩƷ���вɹ��ȷ��治��ѡ��δͨ��һ�������۵�Ʒ�֡���һ��������Ҳ���ڶ�ر�����ԭ�о��۲�Ρ�
������ANDA��ô�࣬NDA��ʱ������
�������ȥ������ȥ�����й���ҩ��ҵ��������õ�ANDA��֤����Ͳ��ѷ��֣���2012�굽2015�꣬���й�ҩ���ANDA�ķ�֤��������ȶ���ÿ������������漰��ҵ����������ȫ��ͬ������2016�꿪ʼ������ˮƽ����һ����Ϊ���Ե���ߣ�2017�������ˡ�
�������Ȼ��һ�����£�����ζ���й���ҩ��ҵ����ҩˮƽ�Ѿ�����õ�ȫ�������г����Ͽɣ��й�ҩ����ȫ���г��ľ�����Ҳ��ʼ���֡������ͬʱ��������һ�����ܺ�����ҩˮƽ�뾺������ָ��������ȴһֱû��ͻ�ƣ�NDA������ҩ���롣
������Ϊ������֪�ģ�Ӧ��������ʿ���ĸ������ε��裬�����1997��12��9������ʽͨ������FDA��ҩ�ٴ��о�������IND����ʼ��������������NDA֮·�Ѿ����˳�����ʮ�꣬�������������ٴ��������Ĺ������������ε����ܷ��������������NDAҲ��Ϊ��ҵ�����۵��ȵ㡣
����������һ������Ϊ���۵�������Ҷ��ҩ��505��b����2����Ʒ����ͪ��������ע���Ƽ�����ǰ���������������һ��������108�����˲���Ĺؼ����ٴ����飬��������FDA��Ϊ������֧����ͨ��505��b����2��;�������ݽ���ҩ���룬����Ϊ���������п������������ҩ������й���ҵ֮һ�������µ���Ϣ�ǣ�FDA�Ѿ���������Ҷ��Ϊ��ҩ���뷽���ύNDA���걨����ʱ�����ύ�Ķ����о��ƻ����⽫���������ҩƷ���з��ɱ����ӿ����е��ٶȡ�
������������ˣ���������ǻ���δ�������κ�һ����ƷNDA��ʽ��ɡ�����������й���ҽҩ��ҵ�У�����ҩ�Ѿ���Ϊ��һ������������������ҩ��������������������������“ȫ����”����һ��ά�������������ڴ���ҩ��ҵҲ������һ��������ǰҹ������ʢҽҩ������ҽҩ�ȶ�ҹ�˾Ŀǰ���в�Ʒ����������IND��
������������Ҳ�������룬2018�꣬���Ǻ��п���ӭ����һ���������õ�NDA�������е��й���������ҩ������ʱ���й���ҩ��ȫ���г��ĵ���ע��������һЩ��
����Ϣ��Դ��Eҩ�����ˣ�Top
2017�꣬CFDA��ǩ��375��ҩƷ���ĺţ���ҽ������������Һ�����ģ�����303�����ģ�163��ҩƷ�����л�ҩռ94.4%��������Ʒ����ҩռ5.6%������ҩռ59.4%������ҩռ40.6%�������ͽ���ҩ���������ӽ���
���������ҹ�һϵ��ҩƷ�������������������ȸ����ƶ���أ�����ҩ�����ٶ����Լӿ졣��Щ������ҩ����������Ҫ�У����Ρ���������������ɭ�������̲�����Ѫѹ������֢�ȡ�
����������2017��26���ص���ڲ�Ʒ�������ͳ�ƣ���26��ҩƷ2016��ȫ�����۶�ߴ�218����Ԫ�����У�6����������ҩ�����۶�Ϊ72.07����Ԫ��8������ҩ���۶�Ϊ69.50����Ԫ��6������ҩ���۶�Ϊ44.06����Ԫ��4��������Ӧ֢ҩ�����۶�Ϊ32.49����Ԫ��
����2017����20�������Ľ�����ҩ�ڹ������У��������ָ����ŵ������˹����������ά����ʱ��ʩ�������¡�ǿ�����ݶ������ϡ�Ĭɳ����ŵ��ŵ�¡���ŵ�Ƶȡ����У����ָ����ŵ���������ڲ�Ʒ��ࡣ������ҩ���������Ժ��ڶ���ڲ�Ʒӿ���й��г�������ҩƷ�г���������ع���
������������ҩ
������������������2017�������е��ص��Ʒ�У���������Ƭ�������ᰢ������Ƭ��άĪ����Ƭ������«������Ƭ��������Ƭ�������ϣ����Ƭ��ע���ð������ա��������ὺ�ң�2016����8����Ʒȫ�����۶�Ϊ69.50����Ԫ��
����Ʒ�֣�
������������Ƭ��2017��2�£�������ʷ�˹�˾��ϸ��������ҩ����������Ƭ�������ڣ���Ʒ��Ϊ“άȫ��”�����Ϊ200mg��400mg��2016����������ȫ�����۶�Ϊ7.29����Ԫ��
���������ᰢ������Ƭ��2017��2�£����ָ���ΰ�����ҩ�������ᰢ������Ƭ�������ڣ���Ʒ��Ϊ“��̩��”�����Ϊ20mg��30mg��40mg��50mg��2016�갢������ȫ�����۶�Ϊ2.71����Ԫ��
����άĪ����Ƭ��2017��2�£����Ϻ�ɫ��������ҩάĪ����Ƭ�������ڣ���Ʒ��“������”�����Ϊ240mg��2016��άĪ����ȫ�����۶�Ϊ2.2����Ԫ��
��������«������Ƭ��2017��3�£�ŵ�����ư�Ѫ��������«������Ƭ�������ڣ���Ʒ��“�����”�����Ϊ5mg��15mg��20mg��2016��«������ȫ�����۶�Ϊ14.34����Ԫ��
��������������Ƭ��2017��3�£��ݶ�θ������������ҩ����������Ƭ�������ڣ���Ʒ��“�����”�����Ϊ40mg��2016��������ȫ�����۶�Ϊ3.04����Ԫ��
���������ϣ����Ƭ��2017��3�£���˹�����ΰ�����ҩ�����ϣ����Ƭ�������ڣ���Ʒ��“̩��ɳ”������ΪƬ�������Ϊ40mg��80mg��2016���ϣ����ȫ�����۶�Ϊ4.23����Ԫ��
����ע���ð������գ�2017��4�£��»���˾��Ѫ������ҩע���ð������ջ������ڣ���Ʒ��Ϊ“ά����”������Ϊ����������Ϊ100mg��2016���ҩȫ�����۶�Ϊ7.38����Ԫ��
�����������ὺ�ң�2017��8�£�����ά��˾��Ѫ������ҩ�������ὺ�һ������ڣ���Ʒ��“����”�����Ϊ140mg��2016����������ȫ�����۶�Ϊ28.31����Ԫ��
����2017��������ڿ�������ҩ��������ҩΪ�������зΰ���Ʒ2�����ֱ�Ϊ��������Ƭ����ϣ����Ƭ����Ѫ����Ʒ3�����ֱ�Ϊ����«������Ƭ��ע���ð������ա��������ὺ�ҡ�������Ʒ�У�2016��ȫ�����۶��10����Ԫ���ذ���Ʒ�����������«�����ᡣԤ��2018��ΰ�����Ѫ����ҩ�г���������һ���Ӿ硣
����������ҩ
������������������2017�������е��ذ���Ʒ�У�����о�Ƭ��������͡����˫��Ƭ��������͡Ƭ�������о�Ƭ���¹��ȵ���ע��Һ�������о�Ƭ����˾����ע��Һ��2016��������Ʒȫ�����۶�44.06����Ԫ��
����Ʒ�֣�
��������о�Ƭ��2017��3�£���˹������˾����о�Ƭ�������ڣ���Ʒ��“������”�����Ϊ5mg��10mg��2016�����о�ȫ�����۶�Ϊ9.07����Ԫ��
����ɳ����͡����˫�һ���Ƭ��2017��9�£����ָ����˾ɳ����͡����˫�һ���Ƭ�������ڣ���Ʒ��“ŷ˫��”�����Ϊ2.5mg/500mg��2.5mg/850mg��2016��ɳ����͡����˫��ȫ�����۶�Ϊ12.49����Ԫ��
����������͡Ƭ��2017��9�£����ָ����������͡Ƭ�������ڣ���Ʒ��“ŷ����”�����Ϊ5mg��2016��������͡ȫ�����۶�Ϊ16.85����Ԫ��
���������о�Ƭ��2017��9�£����ָ�������о�Ƭ�������ڣ���Ʒ��“ŷ�ƾ�”�����Ϊ10mg��25mg��2016������о�ȫ�����۶�Ϊ2.02����Ԫ��
�����¹��ȵ���ע��Һ��2017��9�£�ŵ��ŵ�µ¹��ȵ���ע��Һ�������ڣ���Ʒ��“ŵ�ʹ�”�����Ϊ3ml��300��λ��2016��¹��ȵ���ȫ�����۶�Ϊ6.03����Ԫ��
���������о�Ƭ��2017��9�£�ǿ�������о�Ƭ�������ڣ���Ʒ��“���ɰ�”�����Ϊ100mg��300mg��2016�꿨���о�ȫ�����۶�Ϊ14.07����Ԫ��
������˾����ע��Һ��2017��9�£���ŵ����˾����ע��Һ�������ڣ���Ʒ��“���ɰ�”�����Ϊ10μg����ע��ʡ�20μg����ע��ʡ�2016����˾����ȫ�����۶�Ϊ0.39����Ԫ��
������������������2017���ҹ�������3��SGLT-2���Ƽ�ҩ��ֱ��Ǵ���о��������о��������о���DPP-4���Ƽ������Ƽ���������͡����˫��Ƭ��ɳ����͡����˫�һ���Ƭ��GLP-1�ȸ�Ѫ�����������弤��������˾����ע��Һ����Щ�²�Ʒ�����У���ζ���°е�DPP-4��GLP-1��SGLT-2����ҩ���ѿ��������й����°е�����ҩ��ӿ���г����ؽ����������г���֡�
����������ҩ
�����ڱ�����������2017�������е��ذ���Ʒ�У�������Τ�����ҡ����������ΤƬ��������Τ���ҡ����ײ�ΤƬ���±�����Ƭ��������Τ��Ƭ��2016��������Ʒȫ�����۶�Ϊ72.07����Ԫ��
����Ʒ�֣�
����������Τ�����ҡ�������ΤƬ��2017��4�£���ʱ��ʩ������Τ�����ҡ�������ΤƬ�������ڣ���Ʒ���ֱ�Ϊ“��ά��”��“������”��2016�갢����Τ�ʹ�����Τȫ�����۶�ϼ�Ϊ15.78����Ԫ��
����������Τ���ң�2017��8�£�ǿ��������Τ���һ������ڣ���Ʒ��“����ɭ”�����Ϊ150mg��2016��������Τȫ�����۶�Ϊ1.06����Ԫ��
�������ײ�ΤƬ��2017��9�£����������ײ�ΤƬ�������ڣ���Ʒ��“������”�����Ϊ400mg��2016�����ײ�Τȫ�����۶�Ϊ40.01����Ԫ����ҩ2014��ȫ�����۶�ͻ��100����Ԫ��
�����±�����Ƭ��������Τ��Ƭ��2017��9�£�����ά�±�����Ƭ��������Τ��Ƭ�������ڣ���Ʒ���ֱ�Ϊ“ά����”��“������”�����ֱ�Ϊ12.5mg/75mg/50mg��250mg��2016��±������ʹ�����Τ�ϼ�ȫ�����۶�Ϊ15.22����Ԫ��
�����ڱ�����������2017��CFDA��������Ϳ�������ҩ�ﰢ����Τ��������Τ��������Τ��������Τ���±����������ײ�Τ6����Ʒ���С�Ŀǰ����ʱ��ʩ��ǿ���������¡�����ά�Ŀڷ�������ҩ���ڹ������С������������г������˼��ٱ�����Ѹ��ή��������ŷ��֤ʵ��Ч�����ı�����ҩ֮ս�����ҹ���ʽ���ݣ���Ԥʾ�Ź��ڱ��������������г��������ޱ䡣
������������Ӧ֢
������������Ӧ֢����������2017�������е��ذ���Ʒ�У��ļ�����ͷ���������硢ע���ð����鵥����ɳ�������ɳ̹��Ƭ�����������ҡ�2016������4����Ʒȫ�����۶�Ϊ32.49����Ԫ��
�����ļ�����ͷ���������磺2017��5�£�Ĭɳ����˾�����������ļ�����ͷ����������������ڣ���Ʒ��“�Ѵ���”������Ϊע��������Ϊ0.5mL��2009���ļ�����ͷ����������ȫ�����۶����ߴ�16.61����Ԫ��
����ע���ð����鵥����2017��8�£�ŵ����������ε�ע���ð����鵥���������ڣ���Ʒ��“����”������Ϊ����������Ϊ150mg��2016������鵥��ȫ�����۶�Ϊ23.56����Ԫ��
����ɳ�������ɳ̹��Ƭ��2017��9�£�ŵ��������˥��ҩɳ�������ɳ̹��Ƭ�������ڣ���Ʒ��“ŵ����”�����Ϊ50mg��100mg��200mg��2016��ɳ�������ɳ̹ȫ�����۶�Ϊ1.7����Ԫ��
�����һ������������ң�2017��9�£����ָ����˾���Ʒ���ά����ҩ�һ������������һ������ڣ���Ʒ��“ά����”�����Ϊ100mg��150mg��2016������ȫ�����۶�Ϊ7.23����Ԫ��
����2017�꣬���Ž���ҩע�����ߵĿ��ţ��Խ�����ҩ����б���ȼӴ����������ٶ����Լӿ죬������ҩ���������У����γ�����һ������ҩ�˳���
����Ϣ��Դ��ҽҩ���ñ���Top
2017��7��31�գ�������ʷ�ˣ�GSK�������������������Ĺ���������ϣ��������ʽ���У��������ڵ�ϣ�����Ѿ�ͨ���й�����ʼ첿�ż�����У���Ӧȫ���г���
����������õ�11��9�գ�Ĭɳ���ļ�HPV�������й���½������Ҵ��������Ƿ���������棬�Ƹ�����Ŀǰ���յ�����ʳƷҩƷ�ල�����ܾ�ǩ���ġ�������Ʒ��ǩ���ϸ�֤������Ҳ��ζ��Ĭɳ����9�·��ļ�HPV������ʽȡ��ҩƷͨ�ص����������й��г������˸�Ϊʵ���Ե�һ����
����ʮ��ȴ���һ��������2017��GSK��Ĭɳ���Ĺ�����������̻�������һȫ�������۶10����Ԫ���ذ������Ʒ���ڻ��ֽ��к��±��֣�
����1.GSK��սĬɳ��
����������ʮ����г��ڴ���GSK�Ķ�������ϣ���ʡ�Ĭɳ�����ļ�����Ѵ�������HPV������2017��������У���ζ�����ֽΣ�������������һDZ������г�����ҪGSK��Ĭɳ��������ҵ���г���ֱ�ӽ�����
�����ȴӶ���������GSK����¶����ͳһ�б�۸�Ϊ�����580Ԫ/֧�������������յĸ��Ѽ۸�����ܸ��ݸ������߲������Ƿ�ִ�����۵ȣ������в�ͬ��
��������Ĭɳ�����棬���˽⣬Ĭɳ�����ļ�HPV�����Ѿ���ʼ�ڸ��ز����б꣬�����Ѿ������ϡ����졢���ϡ���������������������6��ʡ���б꣬�۸��Ϊ798Ԫ/֧��������ʡ�ݵ��б깤��Ҳ���ƽ����С�
�������Ӽ۸�������Ĭɳ�����б�۸������7�·��Ѿ���ʼ���۵�GSK����ϣ����580Ԫ���б�۸���ȸ��˽ӽ�40%��������ҵ����ʿ��Ϊ������֮�䲻���пɱ��ԣ���ΪGSK��Ʒ���÷�Χ��9������25���꣬��Ĭɳ����Ʒ�����÷�Χ����20������45���꣬˫����Ҫ�ľ���Ⱥ������20������25���ꡣ
������Ȼ��Ҳ�������ʿ��ʾ��Ĭɳ���ļ۸��ƶ�Ӫ���ռ��������Ը�������Ⱥ��֧������Ҳ��ǿ����ͳ��Ŀǰ�й��ʺ��ļ�HPV�������ȺΪ2.6�ڣ�����Ϊ900����Ĭɳ�����ļ�����Ϊ�����м��㣬���ǵ�Ŀǰ�б�۸�798Ԫ/֧��3��2400Ԫ���������ʴ�30%��Լ��270���ˣ��ò�Ʒ��ģ��65��Ԫ�������Ǵ����г����˴�2%����600���ˣ��г���ģ����130��Ԫ��
���������ߵľ������ǽ������ڼ۸�֮�ϣ����ڹ������ķ�����������һ����Ҫ�Ŀ��˱�����Ϊ������в��Ů�����ij��������������ҹ�Ŀǰÿ�깬�����·�����Ϊ10����������3����15����44��Ů���е�����߷���֢����Ҳ��ҵ��һֱ�������������羡�����е���Ҫԭ��
�����ڴ˷��棬GSKһֱ����“Ԥ������Ч��”��������������GSK��������ʾ����һ���4�ꡢ���鳬��18000�˵�ȫ����ģ�ٴ��о��У�ϣ���ʶ�δ��Ⱦ��Ⱥ����HPV16��18����Ĺ�����ǰ���䣨CIN3+����Ԥ������Ч���ﵽ100%��ͬʱ������������°���HPV�����ý��汣��Ч����ϣ���ʶ������ͱ�HPV�������Ĺ�����ǰ���䣨CIN3+�������屣��Ч���ﵽ��93.2%��
������Ĭɳ���ļ��������߱������ƣ�����Ҫ�����������棬һ�����䣬�����÷�Χ���㣻������Ǽ������ߣ������GSK�Ķ���������˵��Ӧ֢���࣬����ȫ���һ����Ҳ��Ψһ����������Ԥ����HPV6��11��16��18������Ĺ���������ֳ���ٰ�ǰ����İ�֢���磬�������ڹ�����Ԥ�����棬���������õļ�����ͬ��
����ͬ��ֵ��ע����ǣ�GSK��Ʒ�������У�ʵ����ҲΪĬɳ���ļ�HPV���������������г������ڣ�ʹ��Ĭɳ������֮�����Ѹ��չ�����ۡ�����Ӫ�����棬Ĭɳ�������Ƿ������������г��Ķ��Ҵ���Ҳ��һ��������
����2.��ս�ڼ�
���������ȴ�֮��������Ԥ�ڵ����ļ�HPV��������ǩ����Ѹ�١�
������Ĭɳ�����ļ�HPV����Ϊ������ʱ��������2017��5��22�գ��Ѵ�����ʽ��ù���ʳƷҩƷ�ල�����ְܾ䷢��ҩƷע��������2017��9��18�գ���һ������ȡ���˱�����ʳƷҩƷ�ල������ǩ���ġ�����ҩƷͨ�ص�����֮�����м�Ժ��ǩ����һ�㰴�ա�������Ʒ��ǩ�������취���涨���м�Ժ��ǩ������60��������������ɣ����˴�Ĭɳ�����ļ�HPV���绨�Ѳ���2����ʱ�䣬�Ѿ��������г�Ԥ�ڡ�
����������֮������GSK����Ĭɳ������������ͣ��Ŀ�չ�˸��ص��б������ݹ�����Ϣ��Ĭɳ�����ļ�HPV�������ں��ϡ����ϡ����졢������������������������ʡ��ֱϽ�У��б꣬������ʡ��Ҳ�Ѱ���ʡ��Ͷ���չ�ύ�����ύ�����Ͷ�����ϡ�
����GSK��������ʾ������2017��8�·ݣ�ȫ���Ѿ��а������졢���ݡ����������ϵ����ڵ�17��ʡ��ֱϽ�п����������б괰�ڣ�����ȥһ��ʱ����GSK�������ϣ����������17��ʡ�ݵ��б��빤����
��������֮���������б꣬���ƶ��������ۣ���������������ձ�������̣�����ڸ�ʡ����б���֮���������ǵȴ����ظ���ʵ�ʽ��������������Ķ�����“���Ǹ��ݸ��ط����ؼ��ص�λ�Ķ������ڻ���������ͬʱ����δ�б�ĵ���������Ҳ�ڻ������벹�깤������������Ů�ԵĽ�������”GSK�����ʾ��Ŀǰ�Ѿ�����ȫ������״̬����ȷ�������������ڸ��صĹ�Ӧ��
�������������Ҳ�Ʒ��½�����У�GSK��Ĭɳ����ս���Ѿ���ʽ���졣�������һ����������ҵͬ��ԾԾ���ԣ�����HPV�����з�����ҵ���ľ����ѿ��Ƽ��ҡ�
������ͳ�ƣ�Ŀǰ�ҹ��Ѿ���11��ҩ��ݽ���HPV������ٴ����룬�����ļ�����3�ң���������1�ң��ż�����4�ң�����Ĭɳ���ľż�����Ҳ�������С�
����“ҩ���ٴ�����Ǽ�����Ϣ��ʾƽ̨”��ʾ��Ŀǰ�����ɶ��������������Ϻ�����������̩�����Ϻ���Ψ����ȶ�ҹ�˾���ڶ�����HPV��������������ڽ���֮�У���ɭ������ӹ�˾�Ϻ�����Ŀǰ���Ѿ���ʼ�������ٴ���������չ��������ռ������Լ��ٴ��������Ĺ��������з��ľż�HPV�����ٴ��о�����Ҳ�ѻ�����������Ŵ�ѧ���������������\����˾�������еĶ���HPV���������ٴ�����Ҳ���ڽ���֮�С�
����ֻ�ǣ�Ŀǰ������Ա���ҩ������ľ�ѹ������Ϊ�����г�Ԥ����������ɭ�����Ϻ������HPV�������Ҳ��2019������У���ʱ��GSK��Ĭɳ���Ѿ�ռ���г��ߵ㣬��Ҫ��δ�����侺������۸�ս����������¡�
����Ϣ��Դ��Eҩ�����ˣ�Top
�Ϻ�ҽҩ�չ��������й�������ҵ�о���ʿ����������ʾ���Ϻ�ҽҩ���������������“����ս”һ��������
����������ҩ�չ������ֵı�����ҽҩ��ͨ��ͷ����ı�������ǧ�ڲ��ݺ��ӵĴ��������г���
����Ŀǰ������DTPҩ����ģ�Դ����Σ�2015�����۹�ģԼ80��Ԫ��2016���ѳ�������Ԫ��
����ƽ��֤ȯԤ�⣬ҽҩ����������2017���ܹ����еĴ���������������900��Ԫ��2020���г��ռ�Լ6100��Ԫ��Ԥ�ƴ���ҩ����Ҫ����DTPҩ����Ժ�ߵ꣬DTPҩ���г�ռ���ʽ��ߴ�54%��
���������߶������ã�DTPҩ������
����2018��2��2�գ��Ϻ�ҽҩ����ƣ�ȫ���ӹ�˾Century Global���ֽ�5.76����Ԫ�չ��������������Dz���ɽ������ͨ���������������Ǽ��ӵ�������й���ۼ��ڵ�������ȫ���й�ҵ��ʵ�壨�������й�����
��������������ʾ���������й�ӵ��14������ֱ����˾������ȫ��13���ص���У��μ����縲��322�����У������11000��ҽ�ƻ�����ͬʱӵ��30��DTPҩ����
����������֪���������й��ľ���������Ҫ������DTPҩ���ϡ���Ϥ���������й�30��DTPҩ��Ŀǰ�����۶�ɴ�6��Ԫ��7��Ԫ���������۶�һ���ܴ�2000��Ԫ������ͨ����ҩ�굥�����۵�40����ÿ���������Լ15����20���˴Ρ�
����DTPҩ��ģʽ����ҩ������ҩ��ҵ��Ʒ����Ȩ��������ҽԺ��ô������ҩ��ֱ�ӹ���ҩƷ�����רҵָ��������ģʽ���������Գ���OTCҩƷΪ���Ĵ�ͳ����ҩ�꣬DTPҩ����Ҫ���۸�ë��רҵҩ�����ҩ���Է�ҩ��ҩƷ��������ҩ��Ľ���ģʽ��
����2017����ҽ�Ĵ��꣬���������DTPҵ��ķ�չ������ҽԺ�ĸ������ƽ�ҽҩ�ּ����ƵĽ�һ����ʵ�����ؼ����б���ҽ��̸��Ʒ���ƶ�ҩƷ���ۣ����Ƹ�ֵҩƷ���������նˣ�ҩ���ƶȵĸĸ������ҩ���з���Ҳ��������ҩ������������2017���°�ҽ��Ŀ¼�����������ҩ��Ʒ���ش���ҩ����ҽ��Ŀ¼���������DTPҩ����ͨ������֧������Ƿȱ�����⡣
�����ڹ��⣬����ҩ���������ĸı�Ҳ������ҽ�����ߵĸı䣬ҽҩ�ֿ��ķ�չ���Լ������м��̻��ڽ��ͳɱ��ȡ�
������ʵ�����Ⲣû����ν��DTP/DTCҩ����DTP/DTCֻ��һ�ִ���ҩƷ���ṩ���������ı䣬һ�����γ��̵�ҩƷ���Ͳ��Ըı䡣Ϊ��Ӧ�����������뽵���м��̻��ڣ�Խ��Խ��Ĵ���ҩ��ҵ���̲�ȡ��DTP/DTC�����Ͳ��Ըı䣬ת��ֱ����ҩ������������ҩ��ֱ���ṩ������ҩƷ��������
����ҩ��Ҳ����Ѱ���빤ҵ���̺����Ļ��ᣬ����ȡ���̵Ľ�������֧�֣��������������ҽԺ�ͷų������Բ�������������
�������й���DTPҩ����������Խ��Խ������й�˾��Ŀǰ�������Ϻ�ҽҩͨ���չ��������������Ǽ���DTPҩ���⣬���й�ҩһ�¡�����ҽҩ��һ������ҽҩ��ͨ���й�˾��ƾ����Ʒ�ּ��۸����Ʋ���DTPҩ����
�������⣬���ҩ�����ϰ��ա�һ���õ�������Ӫ����ҩ��Ҳϣ����������������������DTPҵ�������ܹ������ն��г���Ʒ��ЧӦ���������ơ�
������ҩ����ռǧ�ڴ��������г�
����DTPҩ��Ϊҽҩ��ҵ�ṩҽҩ�ּҺ��ҩƷ����������ϡȱ��һ�ֻ�����ҩ��Ϣ��DTPҩ��������ҽԺ�����Ĵ�������ҩ�������е��˲�����������ְ�ܣ�������ͨ��ְҵҩʦΪ�����ṩ���Ի���ҩ�����רҵ���������ͷ���
����DTPҩ���ij��֣���ҩƷ����ģʽ�ϣ���������¸ı䣺
����һ��ʵ��ҽҩ�����������ڽ�������ѡ�����������⣻
������������ҽԺ����ҵ��ҵ���Ի����ṩרҵ�����ܸ��õ�ָ�����ߺ�����ҩ��
����������Ϊҽҩ��ҵ����������ͨ�м价�ڣ������˻��ߵ���ҩ�ɱ���
����Ŀǰ������DTPҩ����ģ�Դ����Σ�2015�����۹�ģԼ80��Ԫ��2016���ѳ�������Ԫ��ƽ��֤ȯԤ�⣬ҽҩ����������2017���ܹ����еĴ���������������900��Ԫ��2020���г��ռ�Լ6100��Ԫ��Ԥ�ƴ���ҩ����Ҫ����DTPҩ����Ժ�ߵ꣬DTPҩ���г�ռ���ʽ��ߴ�54%��
����Ŀǰ�����ڵ�DTPҩ����Ҫ��Ϊ���ࣺ
������һ������ҩ����ҩ������������ҵ��˾�����DTPҩ������ҵ��˾�빤ҵ�������ܣ��������Ϻͼ۸��������бȽ��������ƣ����籱��ҽ��ȫ�¡�����ҩ�����Ϻ���Эҩ�ꡢ�����ִ�ҩ���ȣ�
�����ڶ���������ҩ�����裬�ϰ��ա�һ���á�������ҩ����
�����������ǵ�����ҵ���ģ�����Ҳ������ҩ�����罡������������ҩ�����ֺ�Ҳ�����˿�ʼ����DTPҩ����
�����Ϻ�ҽҩ����ҩһ�¡�����ҽҩ��һ������ҽҩ��ͨ���й�˾ƾ����Ʒ�ּ��۸����ƣ���������DTPҩ����
�����Ϻ�ҽҩ�ڻ���������������ӵ��40���DTPҩ�������ϴ˴��չ��Ŀ������й���30��DTPҩ������˾��ӵ�й�������DTPҵ��DTPҩ�����������ù�˾���е�“������”ƽ̨�����Դ��ȫ���ŵ��ռ��Ļ������ݣ�����ҵ�ṩ��Ч��ҩ��Ϣ������ƾ�蹫˾���רҵ���������Ŷӣ���֤����ҩ���͵İ�ȫ�ԡ�
������ҩһ�����µĹ���ҩ��2014����ʽ����DTPҩ������2016�꣬����ҩ��DTPҵ��ͻ��10��Ԫ��ҵ��ռ��10%���ϣ��ŵ�����16�ҡ���˾������DTPҵ���Ͻ���̽���������ִ�����������Ϣ���ݹ���ϵͳ������Ӵ����Ǽ�ϵͳ��ȫ��DTP���ݿ⣬�������һ�ֲ���������չ��������ѯ����ҵ��
�������ҩ�����ϰ��ա�һ���õ�������Ӫ����ҩ��Ҳ�ڳ��Խ�������������������DTPҵ����������ն��һ������2015��ר�ų�������ҩ��ҵ������չDTPƷ�֣��нӴ���ҩ����ҵ����2016����������DTPҩ�������ϰ��ղ�ȡֱ�Ӳ����ŵꡢ�չ�������Ȩ���չ���˾���ŵ�ȶ��ֲ�����չ���Կ��������ϣ��漰��������15�ڡ�
�����ɼ���DTPģʽ�����ڶ�ҩ������ǧ�ڴ��������г�����Ҫ��㡣
����Ϣ��Դ���Ϻ�֤ȯ���ȣ�Top
CFDAҩƷ�������ķ����ġ�������������������ҩƷע������Ĺ�ʾ���ڶ�ʮ������������39��������������ҩƷע�����뼰�����������Թ�ʾ���ݹ�ʾ�������˴���ѡ��39��ҩƷ�У�16��ҩƷΪ����ҩ���У�9��ҩƷΪ��ҩ�ٴ���10��Ϊ��ҩ���У�4��Ϊ��������Ӧ֢��
��������һ������CAR-Tϸ��ҩ����ѡ
�����ڵڶ�ʮ�����������������У���ѡ������CAR-Tϸ��ҩ���ǣ��Ϻ�����������Ƽ���������������3��CAR-T�Ʒ����ٴ����롣���������ǣ�ʹ���Ƚ��Ƽ����������������ֶΡ����������������Ƶ�ҩƷע�����롣
�����������ʲ���
����ϸ�����Ƽ�����Ŀǰ����ҽѧǰ���ص㷢չ����������һЩ�������Ѽ����������ṩ����ϣ������������ϸ����������ȡ���µ��о��ɹ���ϸ�����Ʋ�Ʒ���з�������Ҳ�����ܵ���������ҩ��ҵ�����������ĸ߶ȹ�ע��2017��12��22�գ�CFDA������ϸ�����Ʋ�Ʒ�о������ۼ���ָ��ԭ�����У���������ϸ����������ӭ���淶����չ����չ�ٶ�Ҳ���������������CAR-Tϸ��ҩ���걨���ٸ��������з��ٶȣ��г�ǰ��ֵ���ڴ���
��������ϸ�������з���������������Ŀǰ����6�ҹ�˾���ٴ����������������˴���������������ʾ������3�ҹ�˾֮�⣬���У�2017��12��18���Ͼ����������CAR-Tϸ����������Ƽ��������25����������������2018��1��8�ղ���������ϸ��������˾��CD19Tϸ��ע�����2018��1��12���Ϻ����������JWCAR029�ѽ����걨��
������������
����Ŀǰ��ȫ��������CAR-T��Ʒ�������У��ֱ���ŵ����Kymriah��tisagenlecleucel����Kite��ҩ��Yescarta��KTE-C19����Kymriah�����������ƶ�ͯ��������ˣ�2��25�꣩�ļ����ܰ�ϸ����Ѫ����ALL���������47.5����Ԫ��Yescarta�������������ض����ʹ�Bϸ���ܰ����������37.3����Ԫ����ר��Ԥ�⣬�ҹ��������з���CAR-T�Ʒ�ҩ��������3���ڻ������������Ҳ�ή�����ǿɳ��ܵķ�Χ�ڣ�������10��Ԫ���ڡ�
�������������������������ҩ���г��
��������ҽҩ����������ע��Һ�������뱻��������������ʾ��������ζ����������������ҩ���н�������̽Ρ�
������������ȫ�����۹�70��
�����������������������»���̩�˿�����1997��11�»����������У���Ʒ��Ϊ“Rituxan”��1998��6��2�ջ��ŷ��EMA����2001��6��20�ջ���ձ�PMDA����2008��4��21�ջ�CFDA�����У����ɰٽ���������������ŷ�ޡ��ձ����й��г����ۡ��ò�Ʒ��Ҫ���ڷǻ�����ܰ������ܰ�ϸ����Ѫ�������ƣ�Ϊȫ����������CD20�������ҩ�����Ϲ�˾������Ʒ�֣�ӡ�ȡ�����˹�����������������г��Ѿ��м��ַ��Ʋ�Ʒ��
������ȫ����ҩ����ͳ�ƣ�2016���������������۶�Ϊ74.1����Ԫ��ͬ������1%��2005-2016��ò�Ʒ�긴��������Ϊ7.5%��2007���ҩȫ�����۶�ͻ��50����Ԫ��2013-2016������4��ȫ�����۶�ͻ��70����Ԫ����ҩŷ��ר����2015��ʧЧ��������2018��������ר��������
������������������
����������ҽԺ����ͳ�ƣ�����������2016����ҩ���Ϊ9.8��Ԫ����ͬ������23.5%��2005-2016���긴��������Ϊ28.1%���ò�Ʒ��2012��������ҽԺ��ҩ����5��Ԫ���ڹ�������ҽԺ����ҩ���������۶�������һ���ڹ����г��������������£��������ֳ�ǿ��������̬�ơ�
����������������������2000������ڹ������У���Ʒ��Ϊ“����”������Ϊע��Һ�������500mg��50ml��100mg��10ml���֡��ò�Ʒ�Ƿǻ�������ܰ�����“���”����ҩ�����Ϊ���ڽ᳦����һ����ҩ��
�����²�ƷԤ�����ڻ���
����Ŀǰ���������걨��������������ҵ�и��꺺�ء��������硢������������ϸ�����Ŵ�����㽭�����ȡ������������Ǹ���ҽҩ��һ������ӵ���ҩ�Ҳ�ǹ�������������ҩ������ҽҩ���ӹ�˾���꺺����������������ҩ�ۼ��з�Ͷ�볬��3��Ԫ��Ԥ�ƽ���2018���ڻ�������רҵ��ʿԤ�⣬�ò�Ʒ���к��г�DZ���������۶���������30��Ԫ��Ŀǰ����ҽҩ����ӵ���ҩ�ﲼ����ȫ������ҩϵ�д��ڹ���ǰ�У�������Ʒ�ݶӽ�Ϊ�ḻ��
��������������ɭ��ӵ�����ذ�Ʒ��
�������պ�ɭ���ذ�ҩ����Ҷ����������ġ�����ɳ�ࡢά����͡���ڴ˴ι������������������С�δ�����꣬�⼸���ذ�ҩ�ォ����ɭ������һ�ַ�Ծ��
��������ԭ����ЧGLP-1�ذ�
�������Ҷ��������������ɽ��պ�ɭ�����з���1�ҩ�����ڳ�ЧGLP-1���弤�����������ڵ�ҩ�������˫����������2�������ò�Ʒÿ��ֻ��ע��1�Ρ�
����2007��3�£���ɭ�����걨�������Ļ�ҩ1.1����ٴ��о���2008��10�»���ٴ�������2015��1�¡�7�����������Ҫ�Ģ����ٴ����飻2017��10�¿�ʼע��������2017��12��6�ս����������ģ�2018��1�±������������������ͬʱ����������2008����ѡ����“863�ƻ�”��2010��2012�����λ�ù��ҿƼ��ش�ר��֧�ֵȡ����պ�ɭ��Ʒ�ִӳ����걨�ٴ������������������Ѿ��߹��˽�11����ͷ��
��������Ŀǰ��ȫ����7��GLP-1���弤������ҩ�����У����У�����³�ġ��������ġ�����³���Լ�ע���ð����������Ϊÿ��ע��1�εij�ЧGLP-1���弤������ֵ��һ����ǣ�2018��1��4�գ�������ҩ��GLP-1���弤����ע���ð�����������CFDA�����У�����2���������ơ��ɴˣ�������ҩ��ע���ð����������Ϊ�������������еij�ЧGLP-1���弤������Ȼ����ҩ������������ҩ�����з��ģ�2016��������ҩ�밢˹�������ս�Ժ�����������ҩӵ��Byetta/���ڴ��Bydureon/�ٴ�����й�������ҵȨ�������պ�ɭ�����������ǹ�����ЧGLP-1���弤������ҵ����ʿ���Ƹ�ҩ���罫��2018��������Ȼ�����
��������ɳ��������
��������ɳ���ɰ�ʱ��ʩ������2013��1�»����й�ע�ᣬ��Ʒ��Ϊ“������”����Ҫ�����Źؽڻ�ϥ�ؽ������û����ij��껼��Ԥ������Ѫ˨˨��֢������ΪƬ�������Ϊ2.5mg��2016�갢��ɳ��ȫ�����۶�Ϊ33.43����Ԫ����2015������80%�����۶������������Ѹ�͡�
�����ݹ�������ҽԺ����ͳ�ƣ����ڰ���ɳ���г���ģ��2013���116��Ԫ������2015���510��Ԫ��2016����2015�������ƽ��2017�꣬����ɳ���������°�ҽ��Ŀ¼��2017��1-3���ȸ�ҩ���۶��Ѵ�534��Ԫ��
����������CFDA���ݿ⣬Ŀǰ�����걨����ɳ���Ƽ�����ҵ�н�30�ң���Ҫ��ҵ�н��պ�ɭҩҵ���Ͼ���ŵ����Ƽ�����������ҩҵ����³��ҩ�����ϣ����㶫������ҩҵ��ɽ����ʱ��ҩҵ�ȡ���ʱ��ʩ�İ���ɳ���ڹ�������Ļ�����ר��2022�굽�ڡ����˽⣬�˻�������������Ч����һ��ר������Ч������ɭ�ĵ���Ʒ�ֽ���һʱ������г������������������ҵ����
����ά����͡DPP-4��
����ά����͡��ŵ����ҩ�з���2007��9��28�գ�ά����͡���ŷ��������Ʒ��Ϊ“Galvus”��������ŷ�˹��Ҽ�Ų���Ͱ��������С���ȫ����ҩ����ͳ�ƣ�2012-2016���ҩ���۶�ֱ�Ϊ9.10����Ԫ��12.00����Ԫ��12.24����Ԫ��11.85����Ԫ��11.93����Ԫ���ò�Ʒ�������������۶��10����Ԫ��
����2011��8�£�ŵ����ά����͡Ƭ�������ҹ�����Ʒ��Ϊ“��ά��”��Ŀǰ���������ж���DPP-4���Ƽ�����Ҫ��������͡��������͡��ά����͡��ɳ����͡�Ͱ�����͡����Ϊ����ԭ�У������������С�ά����͡2019��ר�����ڣ���ɭҩҵά����͡�ɹ��������ҩ����������������������Ļ�����ɭ������һ�ذ�Ʒ��ά����͡����Ϊ�²�Ʒ��
����2016�꣬��������ҽԺ�����Ƽ�DPP-4���Ƽ����۶�Ϊ1.83��Ԫ�����У�������͡Ϊ8246��Ԫ��ɳ����͡5226��Ԫ��ά����͡3042��Ԫ��������͡1260��Ԫ��������͡561��Ԫ��
����Ŀǰ��ɭ������Ʒ����Ҫ��3���Ʒ��������ζ���˫��Ƭ���������Ƭ���������ػ���Ƭ������Ҫ��Ʒ�У��������Ƭ���ڷ�������ҪƷ�֣���ɭ�������2016������ҽԺ���۶�Ϊ4972��Ԫ���Ǻ�ɭ�ڷ��ڲ�Ʒ�����۶���Ҫ�����ߡ�ά����͡�����»�������Ϊ��ɭ����Ʒ������һ���ذ���Ʒ��
����Ϣ��Դ��ҽҩ���ñ���Top
| 



